Vamos estudar termoquímica, um assunto super importante para o ENEM!... Mostrar mais
Cadastre-se para ver o conteúdoÉ grátis!
Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Knowunity AI
Matérias
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos os tópicos
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos os tópicos
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos os tópicos
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos os tópicos
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos os tópicos
834
•
Atualizado Apr 20, 2026
•
Rafaela Nogueira
@rafaelanogueira
Vamos estudar termoquímica, um assunto super importante para o ENEM!... Mostrar mais
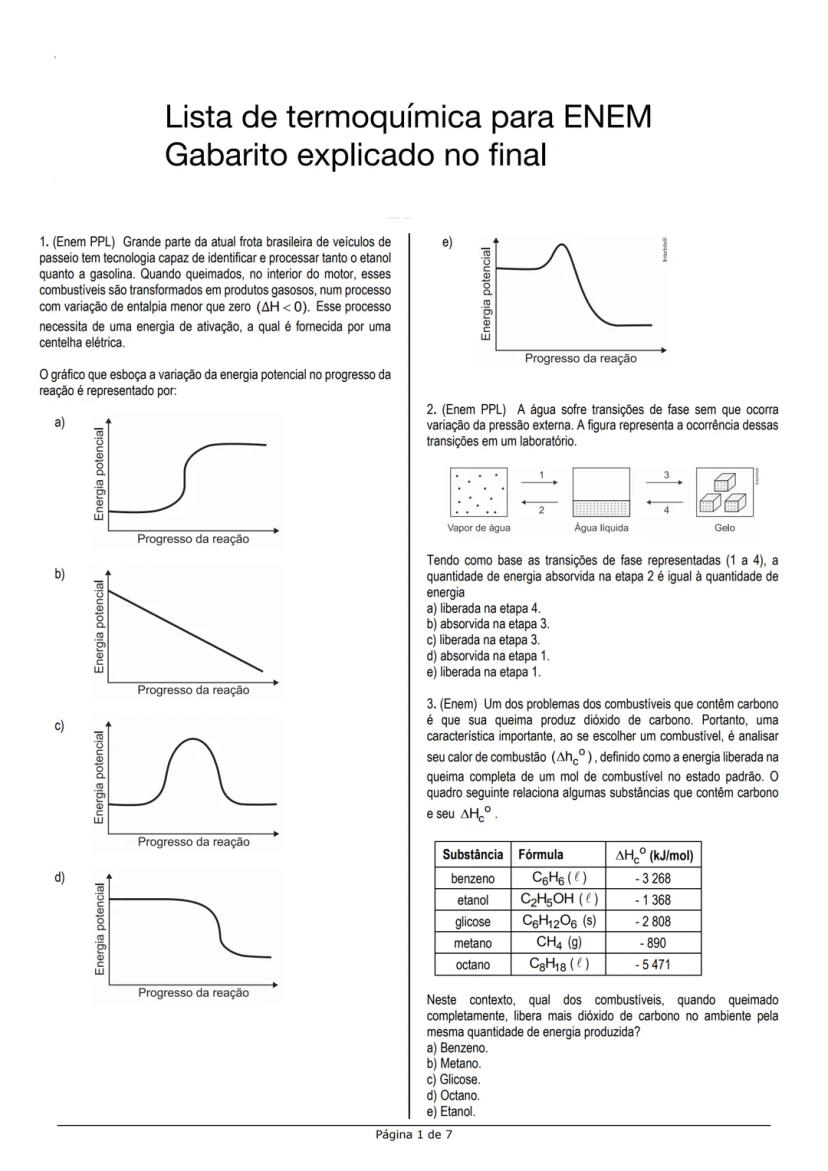




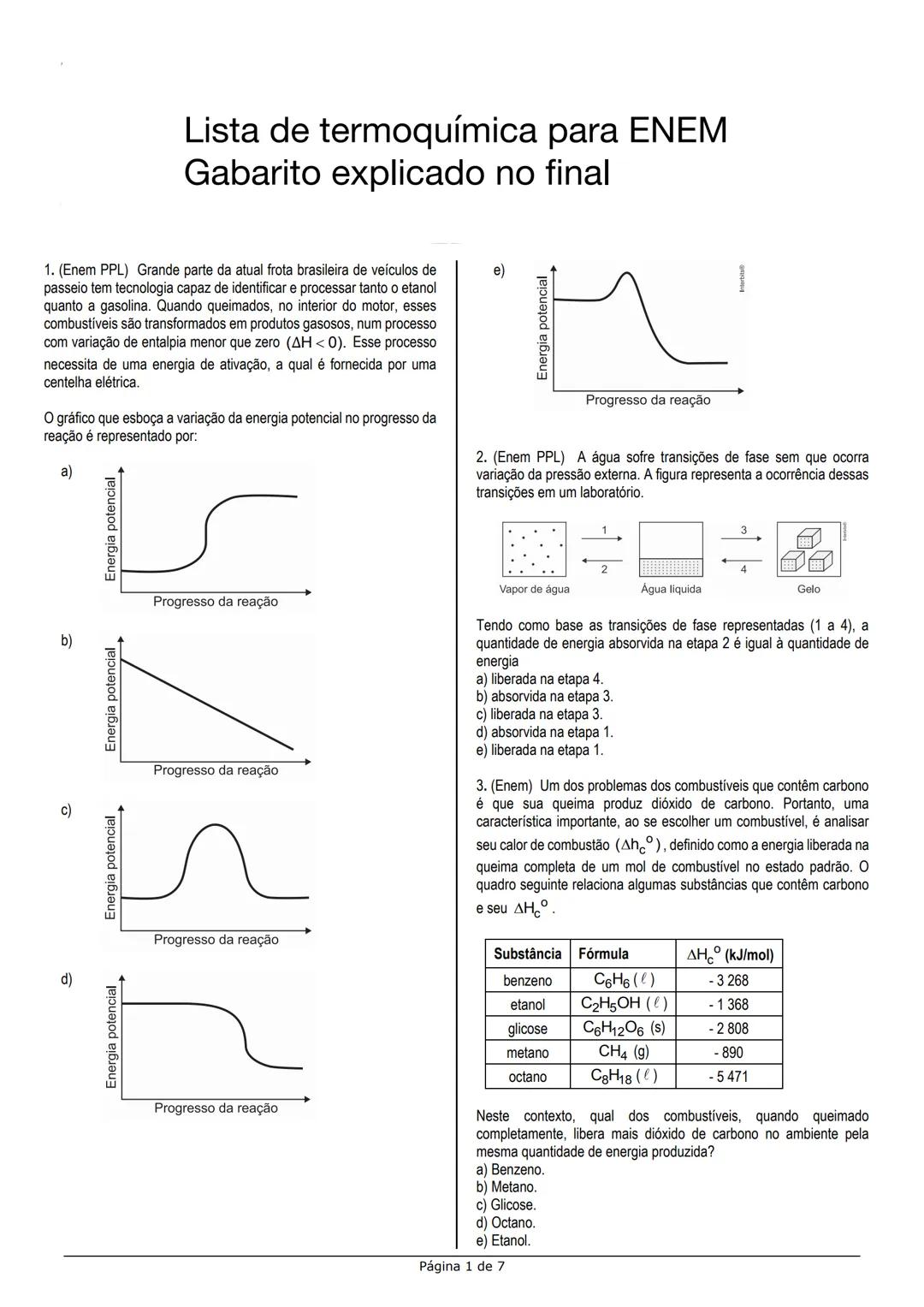
Os exercícios de termoquímica geralmente envolvem o cálculo da energia liberada ou absorvida durante reações químicas. Na questão 1, precisamos entender como interpretar graficamente uma reação exotérmica, que é aquela que libera energia.
Em reações exotérmicas:
Na questão 2, temos um esquema que representa as transições de fase da água. Quando a água líquida vaporiza (etapa 2), ela absorve energia. Esta mesma quantidade de energia será liberada no processo inverso, ou seja, na condensação (etapa 1).
A questão 3 exige comparar a eficiência de diferentes combustíveis. O conceito-chave aqui é entender que precisamos calcular quanto CO₂ é produzido para uma mesma quantidade de energia liberada.
💡 Dica: Em problemas de termoquímica, é fundamental identificar se a reação é exotérmica (libera calor, ΔH < 0) ou endotérmica (absorve calor, ΔH > 0), e saber usar a estequiometria para calcular as proporções corretas.
Para a questão 3, calculamos a quantidade de CO₂ produzida para cada 1000 kJ liberados por cada combustível, descobrindo que a glicose produz mais CO₂ (2,14 mols) para a mesma energia.

A questão 4 trata da glicólise, um processo bioquímico importante que ocorre em nossas células. Aqui, analisamos porque o processo anaeróbico (sem oxigênio) é menos vantajoso energeticamente que o processo aeróbico.
Usando a Lei de Hess (que permite calcular a variação de entalpia de uma reação a partir de outras reações conhecidas), descobrimos que o processo anaeróbico libera apenas 112 kJ por mol de glicose, muito menos que o processo aeróbico completo.
As questões 5, 6 e 7 abordam cálculos energéticos de combustíveis, tema recorrente no ENEM. Esses exercícios exigem que você:
Por exemplo, na questão 7, precisamos comparar o consumo de etanol versus gasolina, considerando:
💡 Quando comparamos combustíveis, é essencial considerar não só o preço, mas também a energia fornecida por litro ou por grama!
Na questão 8, usamos novamente a Lei de Hess para calcular a variação de entalpia na reação de redução do FeO pelo CO. Este tipo de problema exige uma manipulação cuidadosa das equações termoquímicas.

A questão 9 é um excelente exemplo de aplicação da Lei de Hess para calcular indiretamente a energia envolvida em uma reação. Para determinar a entalpia de trimerização do acetileno (formação do benzeno), usamos as entalpias de combustão conhecidas.
Manipulando as equações termoquímicas, conseguimos obter a variação de entalpia para a formação de um mol de benzeno: -150 kcal. O sinal negativo indica que a reação é exotérmica (libera energia).
A questão 10 envolve uma aplicação prática fascinante: os aquecedores químicos usados por soldados para aquecer refeições. A reação entre magnésio e água é exotérmica, liberando 350 kJ de energia. O aquecimento ocorre devido à oxidação do magnésio, que passa de Mg⁰ para Mg²⁺.
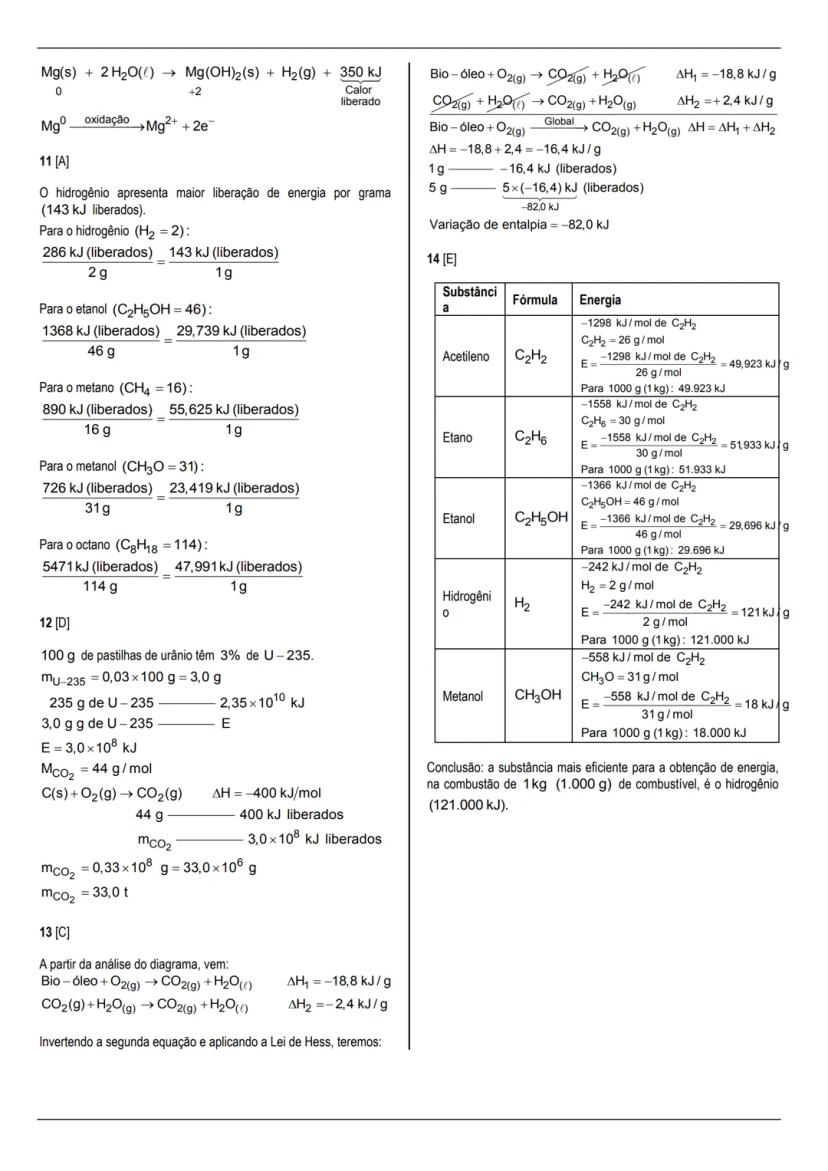
As questões 11 e 13 trabalham com a comparação da eficiência energética de combustíveis:
💡 A análise da eficiência energética considera não apenas a energia liberada por mol, mas também por unidade de massa, o que é crucial para aplicações práticas!
Na questão 13, precisamos calcular a variação de entalpia para a queima de um bio-óleo resultando em CO₂ e H₂O no estado gasoso, aplicando novamente a Lei de Hess.
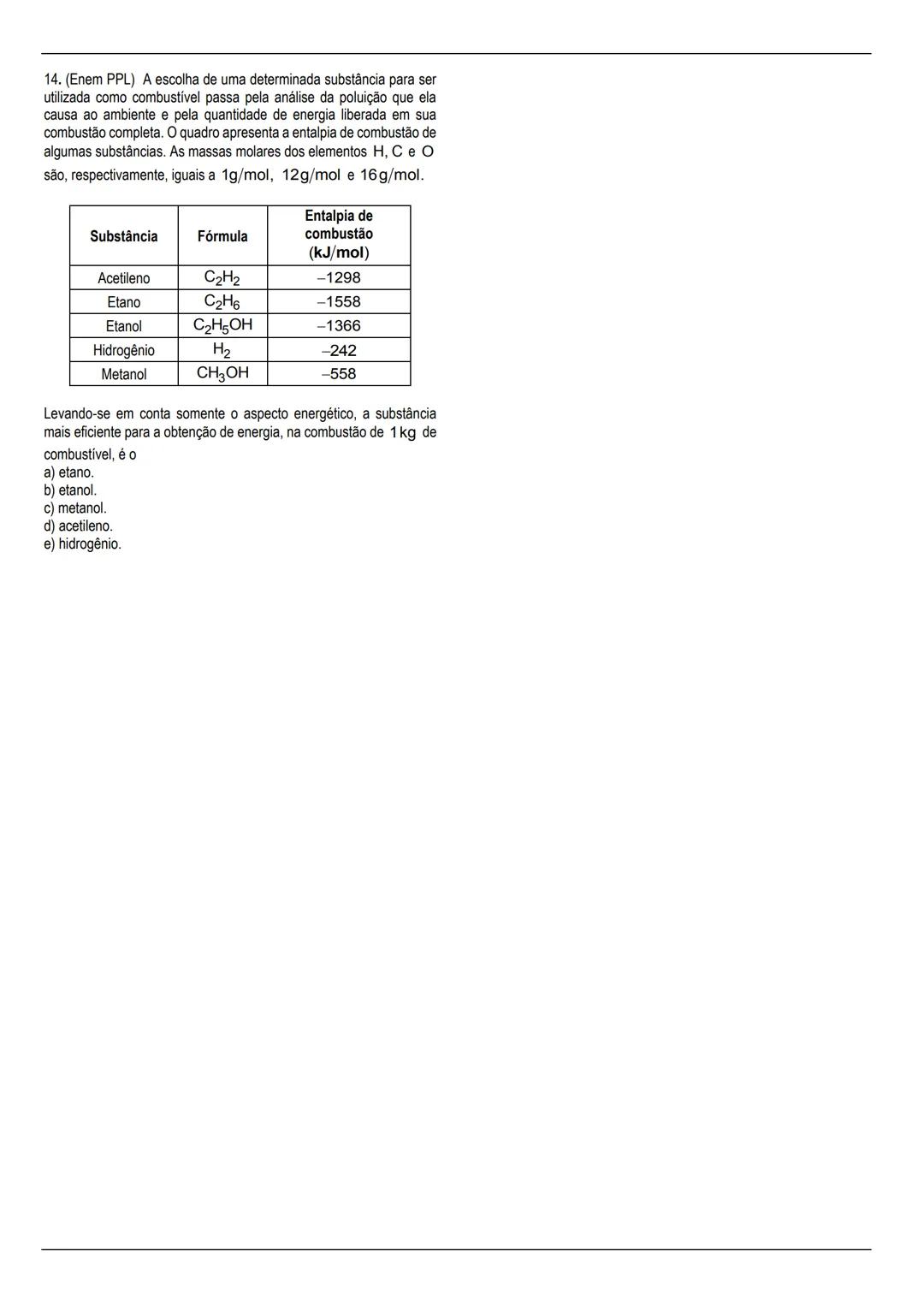
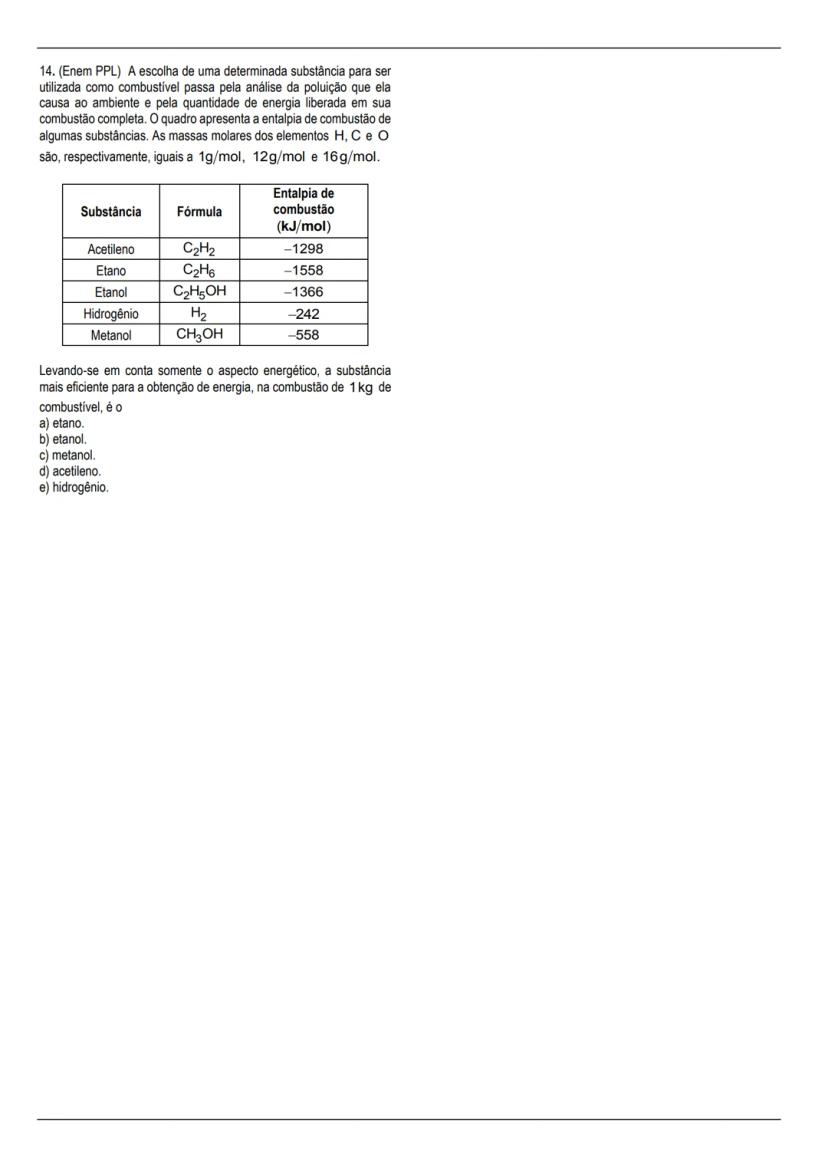
A questão 14 finaliza nossa lista, trabalhando com a eficiência energética de diferentes substâncias como combustíveis. O enunciado apresenta a entalpia de combustão de várias substâncias (acetileno, etano, etanol, hidrogênio e metanol), e precisamos determinar qual é a mais eficiente em termos de energia liberada por kg.
Para resolver este problema, convertemos a energia liberada por mol para energia liberada por grama:
O hidrogênio é claramente o mais eficiente, liberando 121.000 kJ por kg de combustível, mais que o dobro do segundo colocado.
💡 Este é um exemplo perfeito de como a termoquímica nos ajuda a tomar decisões sobre combustíveis alternativos e eficiência energética!
Esta análise é importante no contexto atual de busca por combustíveis mais eficientes e menos poluentes. O hidrogênio é uma opção promissora justamente por sua alta eficiência energética, embora ainda existam desafios técnicos para sua produção e armazenamento em larga escala.

A combustão de etanol e gasolina são reações exotérmicas (ΔH < 0), o que significa que a energia dos produtos é menor que a dos reagentes. O diagrama correto mostra a curva da energia potencial descendo (reagentes → produtos), com um "morro" representando a energia de ativação.
As transições de fase da água seguem princípios de conservação de energia. A energia absorvida na vaporização (etapa 2) é igual à energia liberada na condensação (etapa 1). Este é um princípio fundamental da termoquímica.
Este exercício compara a emissão de CO₂ por diferentes combustíveis. Para cada 1000 kJ de energia liberada:
A glicose produz mais CO₂ para a mesma quantidade de energia liberada, sendo a menos eficiente em termos ambientais.
Comparando o processo aeróbico (com oxigênio) e anaeróbico (sem oxigênio) na glicólise, descobrimos que o processo anaeróbico libera apenas 112 kJ por mol de glicose, muito menos que o processo completo . Por isso é menos vantajoso energeticamente.
💡 Este é o mesmo princípio que explica por que nos cansamos mais rapidamente em exercícios de alta intensidade, quando o corpo passa a usar o metabolismo anaeróbico!

Para um carro que rende 20 km/L, percorrer 400 km requer 20 L de etanol. Com densidade de 0,8 g/cm³, isso equivale a 16.000 g de etanol. Usando o calor de combustão e a massa molar , calculamos a energia: 452 MJ.
Nesta questão sobre o metabolismo da glicose, calculamos que a oxidação de 1 g de glicose libera aproximadamente 6,2 kJ de energia para atividade muscular, considerando que apenas 40% da energia total é disponibilizada para os músculos.
Comparando etanol e gasolina, calculamos que para liberar a mesma energia de 40 L de gasolina (280.000 kcal), precisamos de 58 L de etanol. Isso demonstra a diferença de eficiência energética entre os dois combustíveis.
Usando a Lei de Hess e manipulando as equações termoquímicas, calculamos que a variação de entalpia para a reação FeO(s) + CO(g) → Fe(s) + CO₂(g) é aproximadamente -17 kJ/mol de FeO.
Para determinar a entalpia de trimerização do acetileno (3 C₂H₂ → C₆H₆), usamos as entalpias de combustão e a Lei de Hess, chegando a ΔH = -150 kcal/mol. O sinal negativo indica que a reação é exotérmica.
O aquecimento na bolsa de comida do soldado ocorre devido à oxidação do magnésio, que é uma reação exotérmica que libera 350 kJ. Nesta reação, o magnésio passa de Mg⁰ para Mg²⁺, caracterizando uma oxidação.
💡 Este é um exemplo fascinante de aplicação prática da termoquímica que pode salvar vidas em situações de emergência!
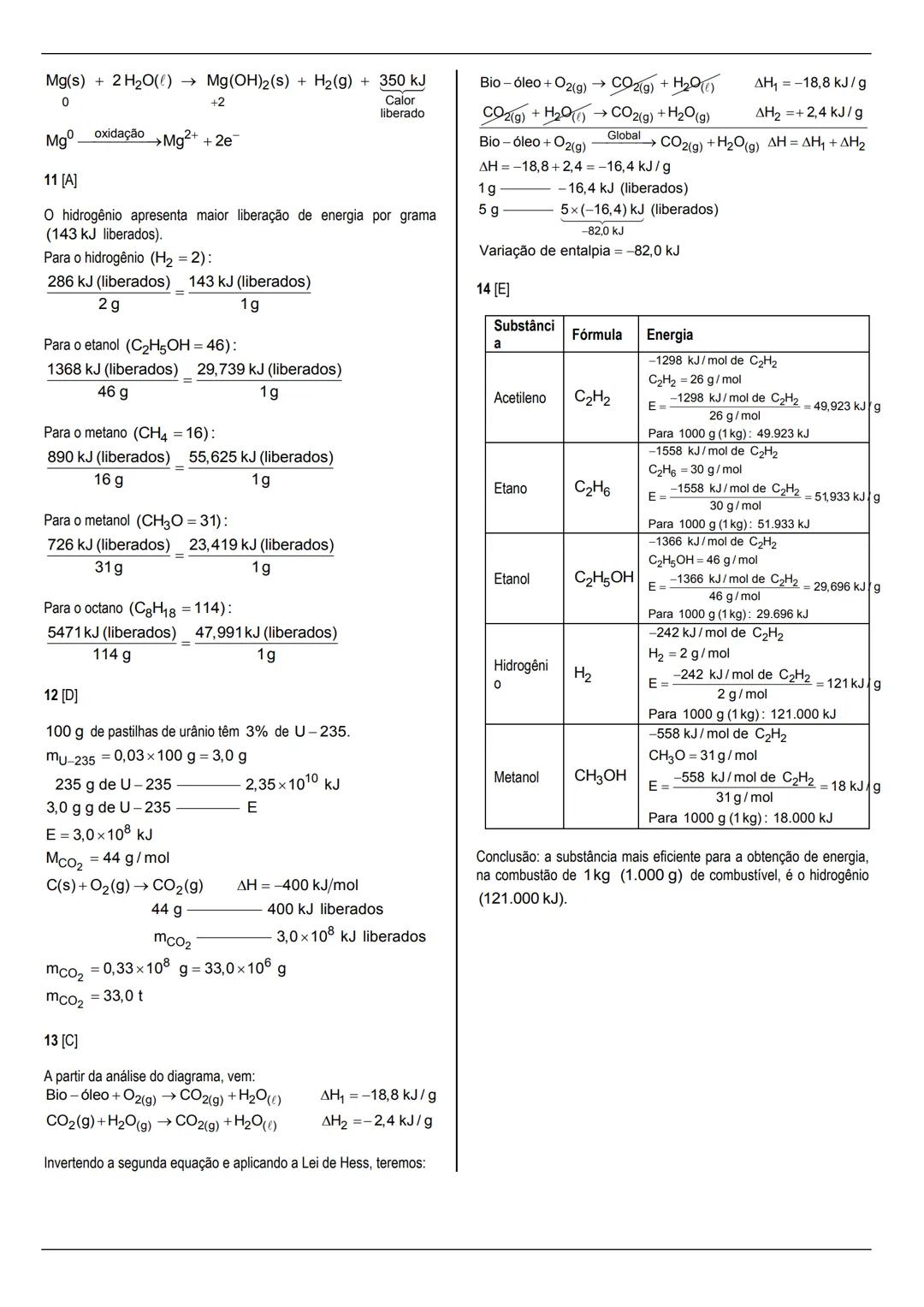
Comparando a eficiência energética de diferentes combustíveis, calculamos a energia liberada por grama:
O hidrogênio é o mais eficiente, liberando 143 kJ por grama de combustível.
Esta questão combina conceitos de química nuclear e termoquímica. Para 3 g de urânio-235 (3% de 100 g de pastilhas), a energia liberada é de 3,0 × 10⁸ kJ. Comparando com a queima do carvão, isso evita a liberação de 33 toneladas de CO₂.
Usando a Lei de Hess para analisar a queima de um bio-óleo, calculamos que a variação de entalpia para 5 g desse bio-óleo resultando em CO₂ e H₂O no estado gasoso é de -82 kJ.
Na análise da eficiência energética por massa, o hidrogênio é o mais eficiente:
O hidrogênio libera mais que o dobro de energia por kg que o segundo colocado, o que explica seu potencial como combustível do futuro.
💡 Isso explica por que muitos consideram o hidrogênio como o combustível do futuro, apesar dos desafios técnicos de produção e armazenamento!
Estes exercícios mostram a importância da termoquímica para entender processos energéticos, comparar combustíveis e avaliar impactos ambientais - todos temas recorrentes no ENEM.
Nosso companheiro de IA foi criado especificamente para atender às necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos oferecer respostas realmente relevantes e significativas. Mas não se trata apenas de respostas, o companheiro também está aqui para guiar você pelos desafios diários de aprendizado, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização com base nas suas habilidades e desenvolvimentos.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
App Store
Google Play
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
Rafaela Nogueira
@rafaelanogueira
Vamos estudar termoquímica, um assunto super importante para o ENEM! Aqui você vai entender como calcular a energia envolvida nas reações químicas, analisar diagramas de energia e comparar a eficiência energética de diferentes combustíveis, tudo com exercícios resolvidos passo a... Mostrar mais

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Os exercícios de termoquímica geralmente envolvem o cálculo da energia liberada ou absorvida durante reações químicas. Na questão 1, precisamos entender como interpretar graficamente uma reação exotérmica, que é aquela que libera energia.
Em reações exotérmicas:
Na questão 2, temos um esquema que representa as transições de fase da água. Quando a água líquida vaporiza (etapa 2), ela absorve energia. Esta mesma quantidade de energia será liberada no processo inverso, ou seja, na condensação (etapa 1).
A questão 3 exige comparar a eficiência de diferentes combustíveis. O conceito-chave aqui é entender que precisamos calcular quanto CO₂ é produzido para uma mesma quantidade de energia liberada.
💡 Dica: Em problemas de termoquímica, é fundamental identificar se a reação é exotérmica (libera calor, ΔH < 0) ou endotérmica (absorve calor, ΔH > 0), e saber usar a estequiometria para calcular as proporções corretas.
Para a questão 3, calculamos a quantidade de CO₂ produzida para cada 1000 kJ liberados por cada combustível, descobrindo que a glicose produz mais CO₂ (2,14 mols) para a mesma energia.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A questão 4 trata da glicólise, um processo bioquímico importante que ocorre em nossas células. Aqui, analisamos porque o processo anaeróbico (sem oxigênio) é menos vantajoso energeticamente que o processo aeróbico.
Usando a Lei de Hess (que permite calcular a variação de entalpia de uma reação a partir de outras reações conhecidas), descobrimos que o processo anaeróbico libera apenas 112 kJ por mol de glicose, muito menos que o processo aeróbico completo.
As questões 5, 6 e 7 abordam cálculos energéticos de combustíveis, tema recorrente no ENEM. Esses exercícios exigem que você:
Por exemplo, na questão 7, precisamos comparar o consumo de etanol versus gasolina, considerando:
💡 Quando comparamos combustíveis, é essencial considerar não só o preço, mas também a energia fornecida por litro ou por grama!
Na questão 8, usamos novamente a Lei de Hess para calcular a variação de entalpia na reação de redução do FeO pelo CO. Este tipo de problema exige uma manipulação cuidadosa das equações termoquímicas.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A questão 9 é um excelente exemplo de aplicação da Lei de Hess para calcular indiretamente a energia envolvida em uma reação. Para determinar a entalpia de trimerização do acetileno (formação do benzeno), usamos as entalpias de combustão conhecidas.
Manipulando as equações termoquímicas, conseguimos obter a variação de entalpia para a formação de um mol de benzeno: -150 kcal. O sinal negativo indica que a reação é exotérmica (libera energia).
A questão 10 envolve uma aplicação prática fascinante: os aquecedores químicos usados por soldados para aquecer refeições. A reação entre magnésio e água é exotérmica, liberando 350 kJ de energia. O aquecimento ocorre devido à oxidação do magnésio, que passa de Mg⁰ para Mg²⁺.
As questões 11 e 13 trabalham com a comparação da eficiência energética de combustíveis:
💡 A análise da eficiência energética considera não apenas a energia liberada por mol, mas também por unidade de massa, o que é crucial para aplicações práticas!
Na questão 13, precisamos calcular a variação de entalpia para a queima de um bio-óleo resultando em CO₂ e H₂O no estado gasoso, aplicando novamente a Lei de Hess.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A questão 14 finaliza nossa lista, trabalhando com a eficiência energética de diferentes substâncias como combustíveis. O enunciado apresenta a entalpia de combustão de várias substâncias (acetileno, etano, etanol, hidrogênio e metanol), e precisamos determinar qual é a mais eficiente em termos de energia liberada por kg.
Para resolver este problema, convertemos a energia liberada por mol para energia liberada por grama:
O hidrogênio é claramente o mais eficiente, liberando 121.000 kJ por kg de combustível, mais que o dobro do segundo colocado.
💡 Este é um exemplo perfeito de como a termoquímica nos ajuda a tomar decisões sobre combustíveis alternativos e eficiência energética!
Esta análise é importante no contexto atual de busca por combustíveis mais eficientes e menos poluentes. O hidrogênio é uma opção promissora justamente por sua alta eficiência energética, embora ainda existam desafios técnicos para sua produção e armazenamento em larga escala.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A combustão de etanol e gasolina são reações exotérmicas (ΔH < 0), o que significa que a energia dos produtos é menor que a dos reagentes. O diagrama correto mostra a curva da energia potencial descendo (reagentes → produtos), com um "morro" representando a energia de ativação.
As transições de fase da água seguem princípios de conservação de energia. A energia absorvida na vaporização (etapa 2) é igual à energia liberada na condensação (etapa 1). Este é um princípio fundamental da termoquímica.
Este exercício compara a emissão de CO₂ por diferentes combustíveis. Para cada 1000 kJ de energia liberada:
A glicose produz mais CO₂ para a mesma quantidade de energia liberada, sendo a menos eficiente em termos ambientais.
Comparando o processo aeróbico (com oxigênio) e anaeróbico (sem oxigênio) na glicólise, descobrimos que o processo anaeróbico libera apenas 112 kJ por mol de glicose, muito menos que o processo completo . Por isso é menos vantajoso energeticamente.
💡 Este é o mesmo princípio que explica por que nos cansamos mais rapidamente em exercícios de alta intensidade, quando o corpo passa a usar o metabolismo anaeróbico!

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Para um carro que rende 20 km/L, percorrer 400 km requer 20 L de etanol. Com densidade de 0,8 g/cm³, isso equivale a 16.000 g de etanol. Usando o calor de combustão e a massa molar , calculamos a energia: 452 MJ.
Nesta questão sobre o metabolismo da glicose, calculamos que a oxidação de 1 g de glicose libera aproximadamente 6,2 kJ de energia para atividade muscular, considerando que apenas 40% da energia total é disponibilizada para os músculos.
Comparando etanol e gasolina, calculamos que para liberar a mesma energia de 40 L de gasolina (280.000 kcal), precisamos de 58 L de etanol. Isso demonstra a diferença de eficiência energética entre os dois combustíveis.
Usando a Lei de Hess e manipulando as equações termoquímicas, calculamos que a variação de entalpia para a reação FeO(s) + CO(g) → Fe(s) + CO₂(g) é aproximadamente -17 kJ/mol de FeO.
Para determinar a entalpia de trimerização do acetileno (3 C₂H₂ → C₆H₆), usamos as entalpias de combustão e a Lei de Hess, chegando a ΔH = -150 kcal/mol. O sinal negativo indica que a reação é exotérmica.
O aquecimento na bolsa de comida do soldado ocorre devido à oxidação do magnésio, que é uma reação exotérmica que libera 350 kJ. Nesta reação, o magnésio passa de Mg⁰ para Mg²⁺, caracterizando uma oxidação.
💡 Este é um exemplo fascinante de aplicação prática da termoquímica que pode salvar vidas em situações de emergência!

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Comparando a eficiência energética de diferentes combustíveis, calculamos a energia liberada por grama:
O hidrogênio é o mais eficiente, liberando 143 kJ por grama de combustível.
Esta questão combina conceitos de química nuclear e termoquímica. Para 3 g de urânio-235 (3% de 100 g de pastilhas), a energia liberada é de 3,0 × 10⁸ kJ. Comparando com a queima do carvão, isso evita a liberação de 33 toneladas de CO₂.
Usando a Lei de Hess para analisar a queima de um bio-óleo, calculamos que a variação de entalpia para 5 g desse bio-óleo resultando em CO₂ e H₂O no estado gasoso é de -82 kJ.
Na análise da eficiência energética por massa, o hidrogênio é o mais eficiente:
O hidrogênio libera mais que o dobro de energia por kg que o segundo colocado, o que explica seu potencial como combustível do futuro.
💡 Isso explica por que muitos consideram o hidrogênio como o combustível do futuro, apesar dos desafios técnicos de produção e armazenamento!
Estes exercícios mostram a importância da termoquímica para entender processos energéticos, comparar combustíveis e avaliar impactos ambientais - todos temas recorrentes no ENEM.
Nosso companheiro de IA foi criado especificamente para atender às necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos oferecer respostas realmente relevantes e significativas. Mas não se trata apenas de respostas, o companheiro também está aqui para guiar você pelos desafios diários de aprendizado, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização com base nas suas habilidades e desenvolvimentos.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
23
Ferramentas Inteligentes NOVO
Transforme esta anotação em: ✓ 50+ Questões de Prática ✓ Flashcards Interativos ✓ Simulado Completo ✓ Esquemas de Redação
App Store
Google Play
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS