A geometria molecular e as forças intermoleculares são temas fascinantes... Mostrar mais
Cadastre-se para ver o conteúdoÉ grátis!
Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Knowunity AI
Matérias
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos os tópicos
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos os tópicos
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos os tópicos
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos os tópicos
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos os tópicos
1,191
•
Atualizado Apr 9, 2026
•
Sophia Lima Sophia
@sophialimasophi
A geometria molecular e as forças intermoleculares são temas fascinantes... Mostrar mais


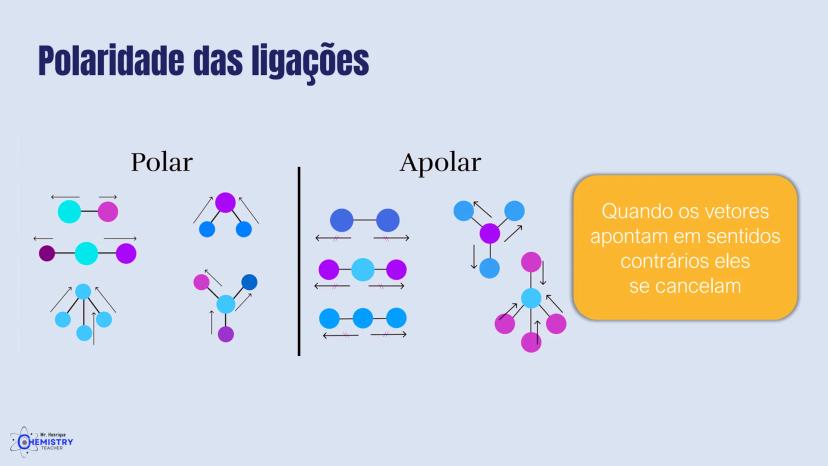

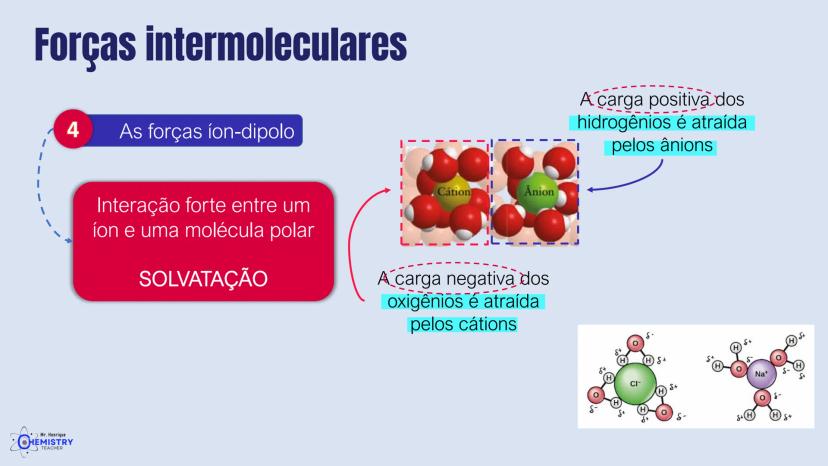
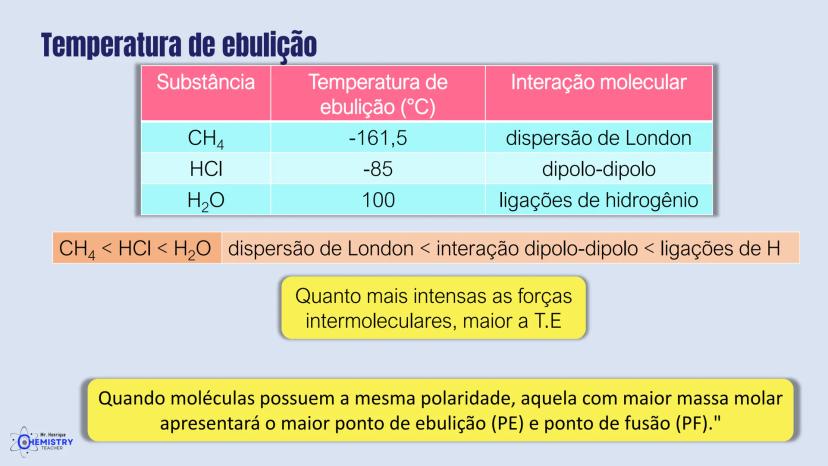

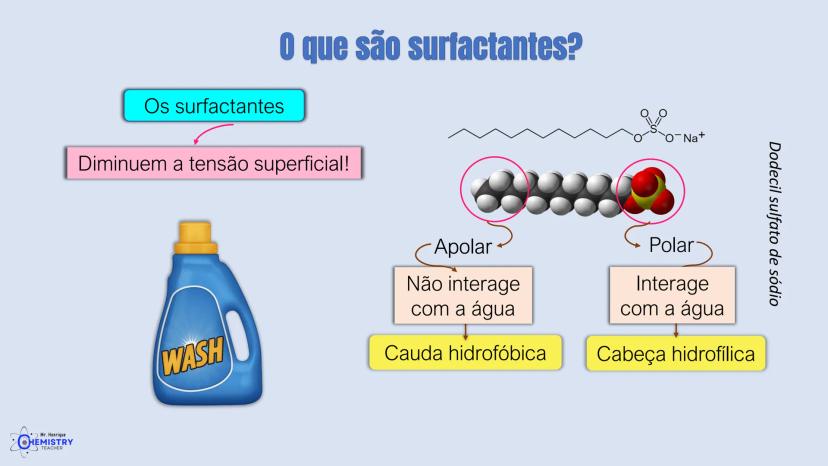
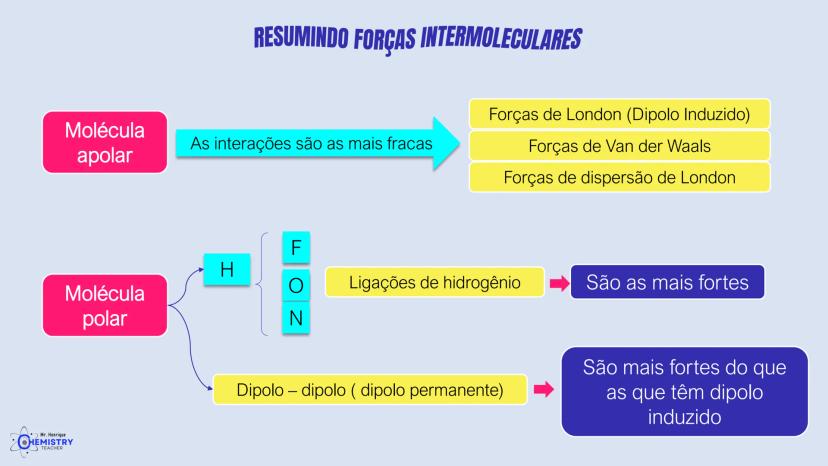

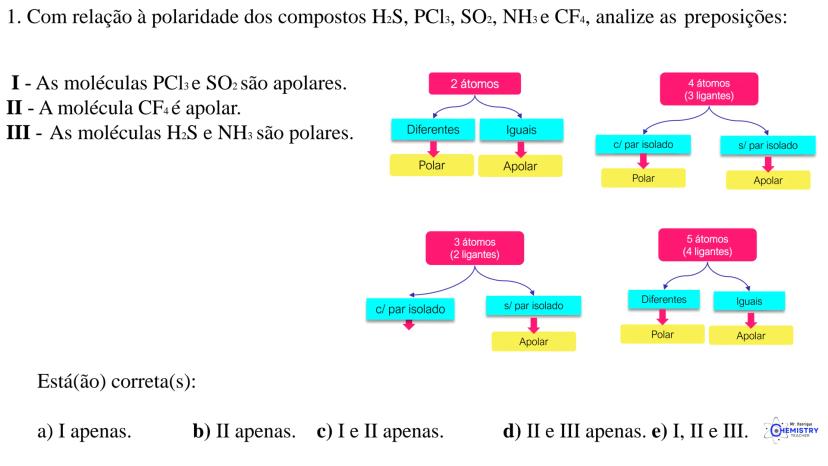
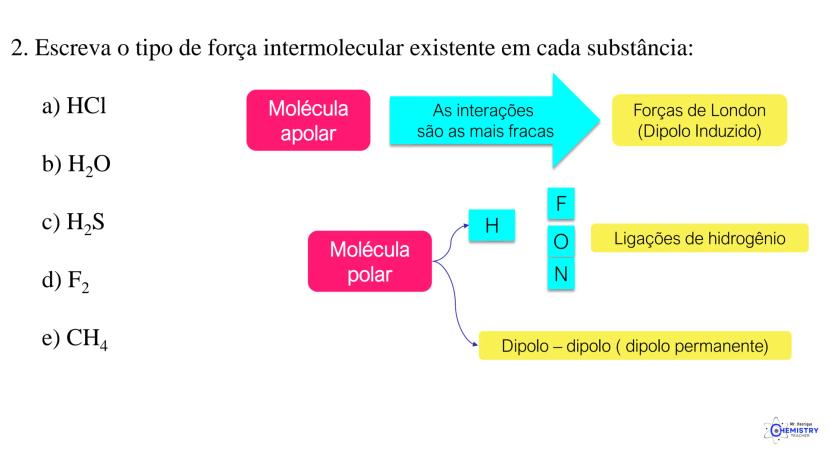
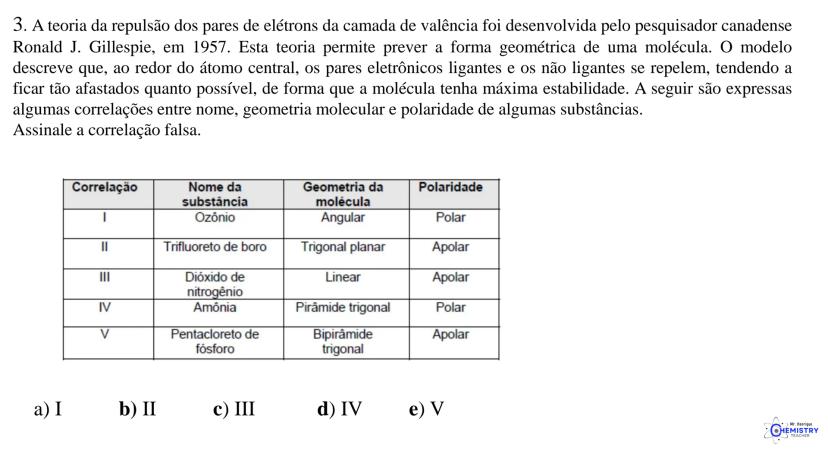
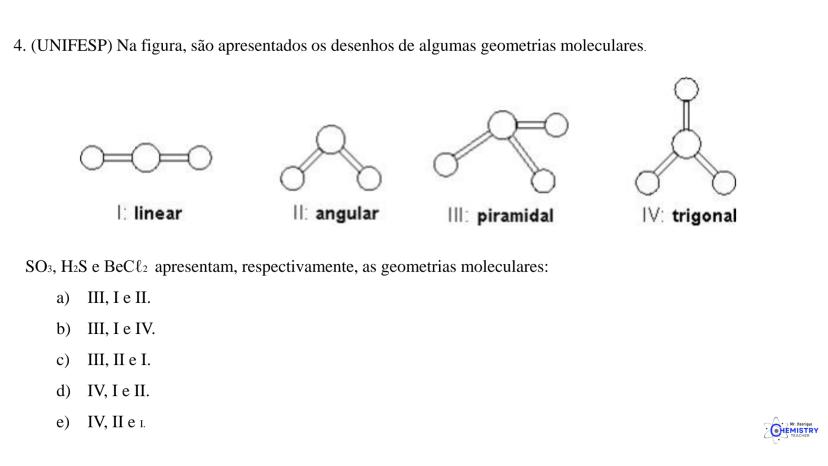




A química do 9º ano nos apresenta um tema super importante: como as moléculas se organizam no espaço! A geometria molecular descreve o arranjo tridimensional dos átomos e influencia diretamente as propriedades das substâncias.
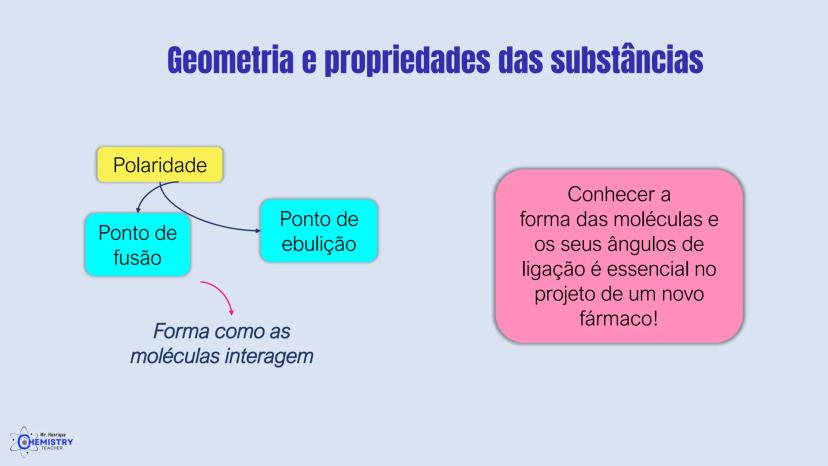
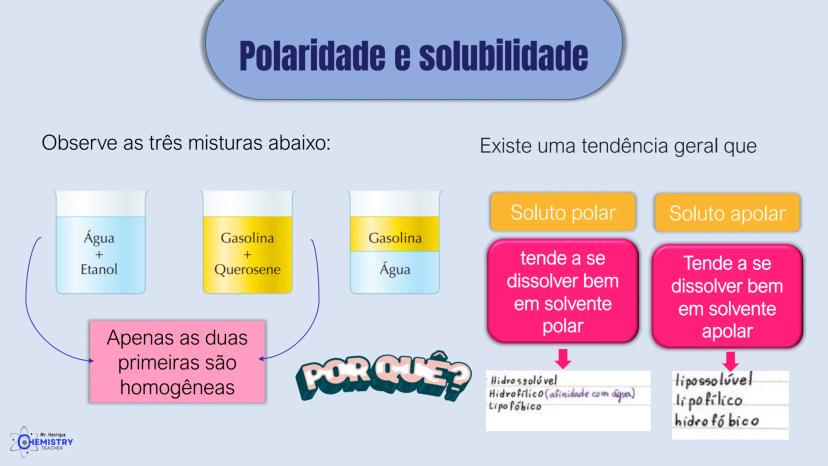
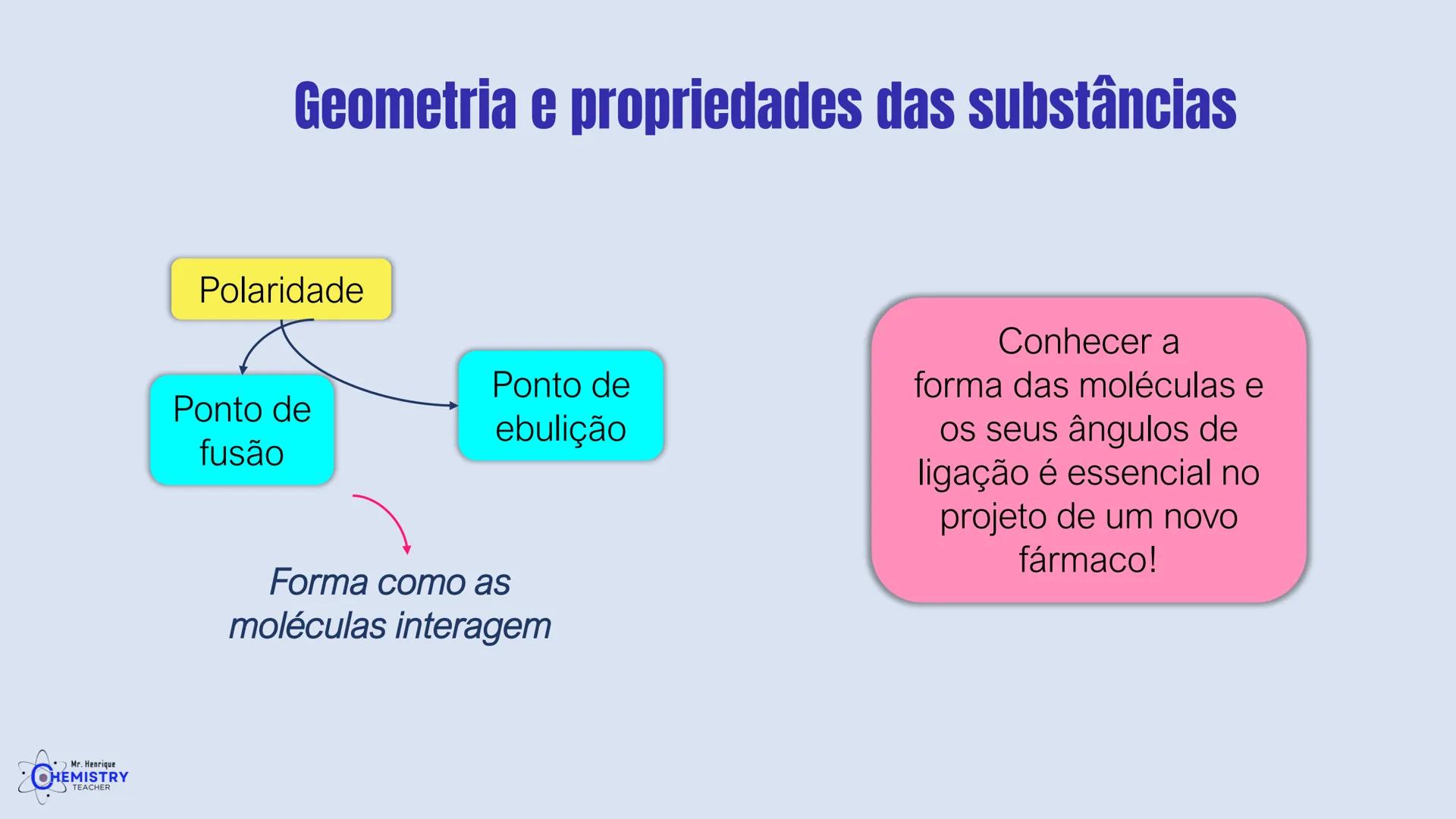
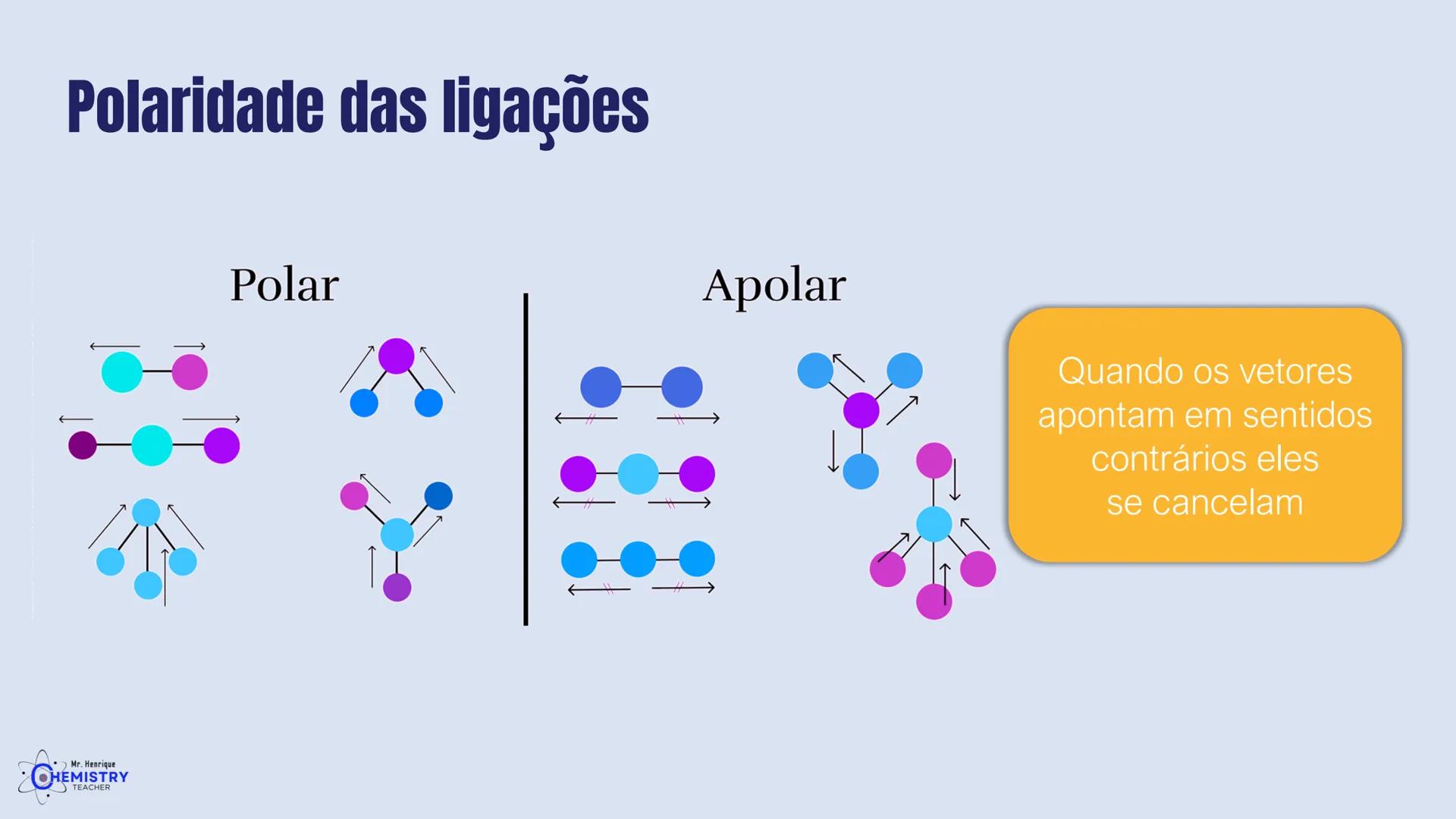
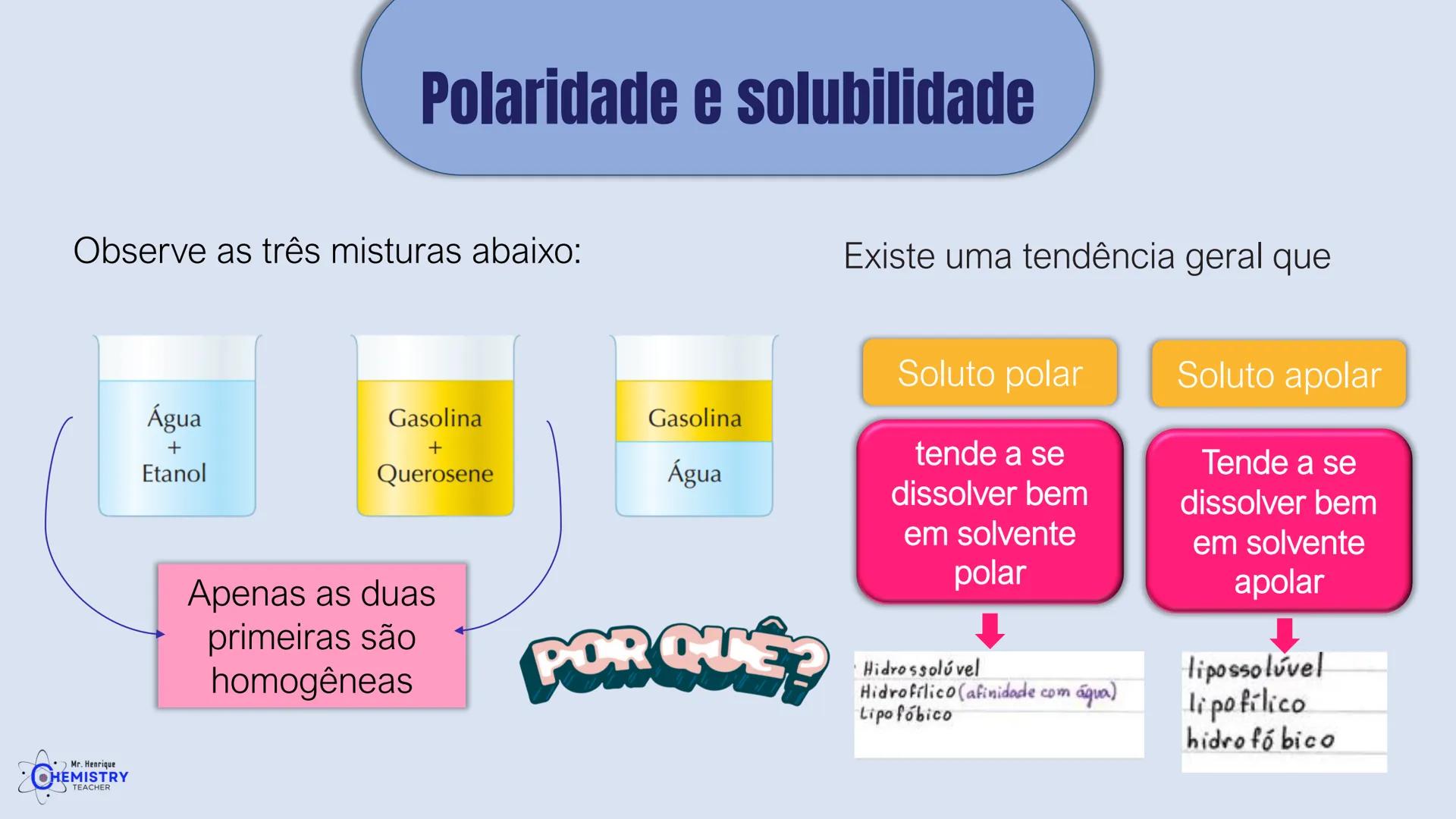
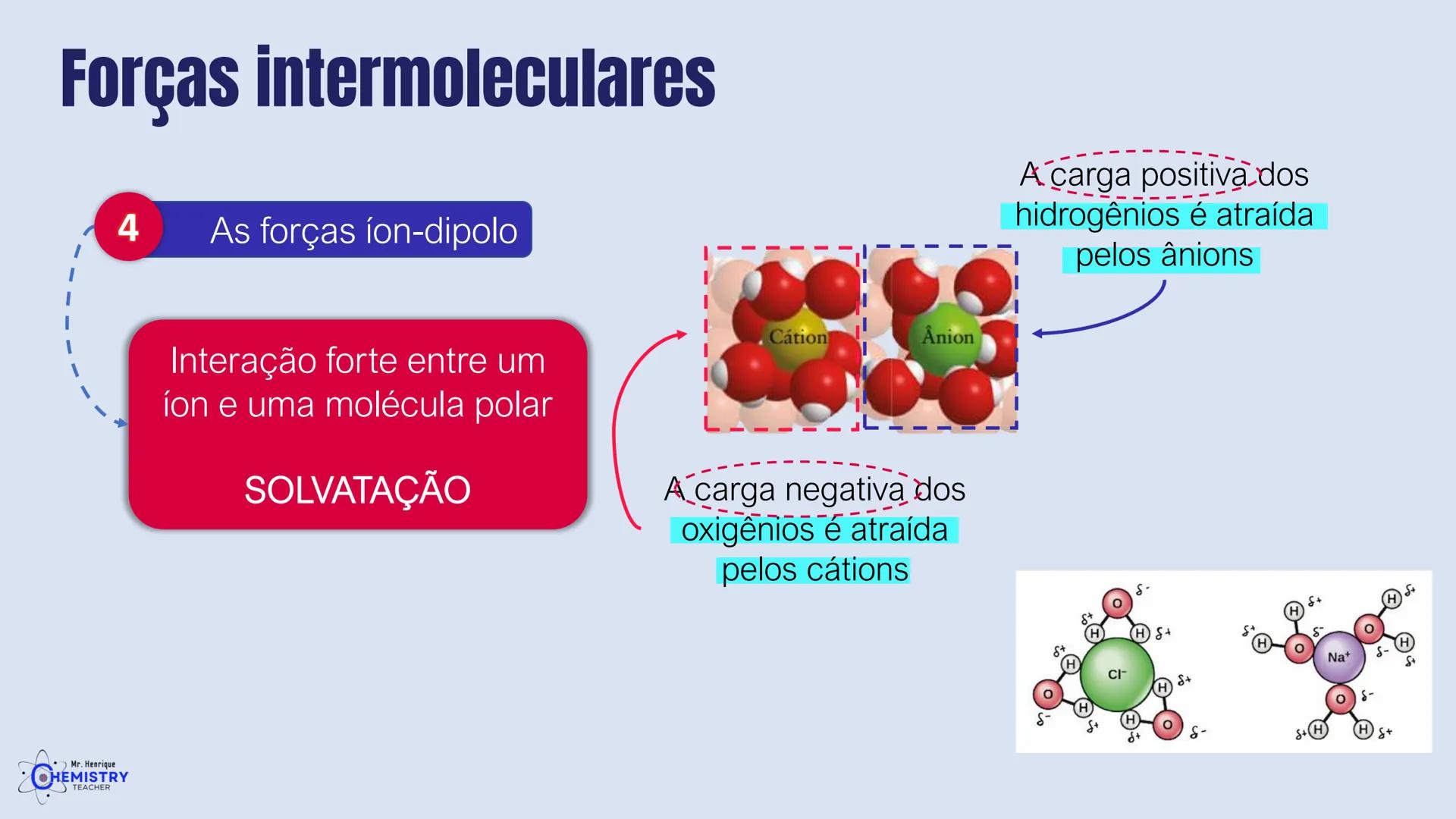
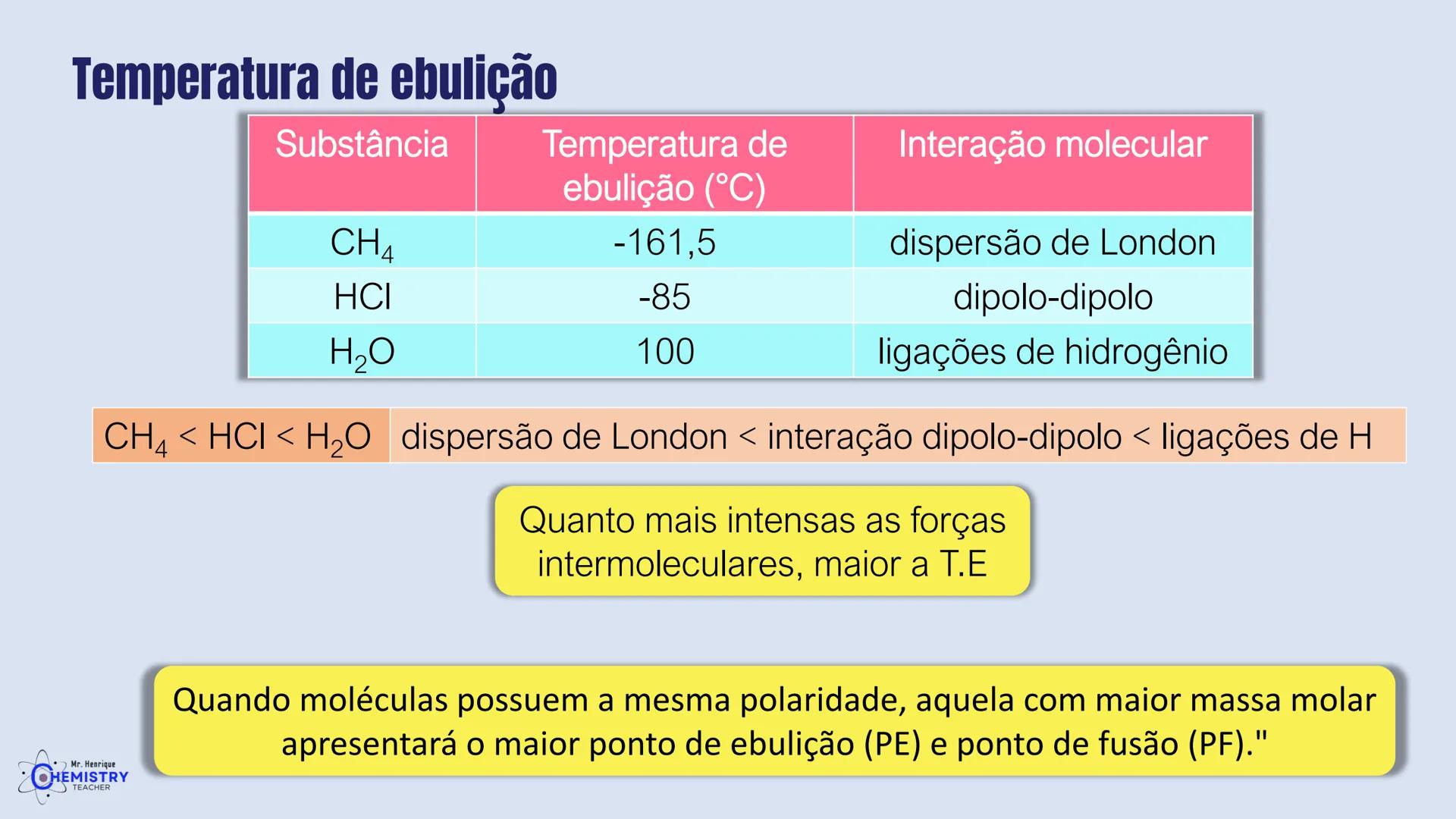
Você já parou para pensar por que algumas substâncias se dissolvem em água e outras não? Ou por que alguns gases têm pontos de ebulição tão diferentes? A resposta está na geometria das moléculas e na sua polaridade.
Neste estudo, vamos descobrir como prever as formas das moléculas e entender como essas formas afetam o comportamento das substâncias no mundo real.
💡 Saber a geometria molecular não é apenas decorar formas! É entender como a natureza organiza os átomos para criar todas as substâncias que conhecemos.
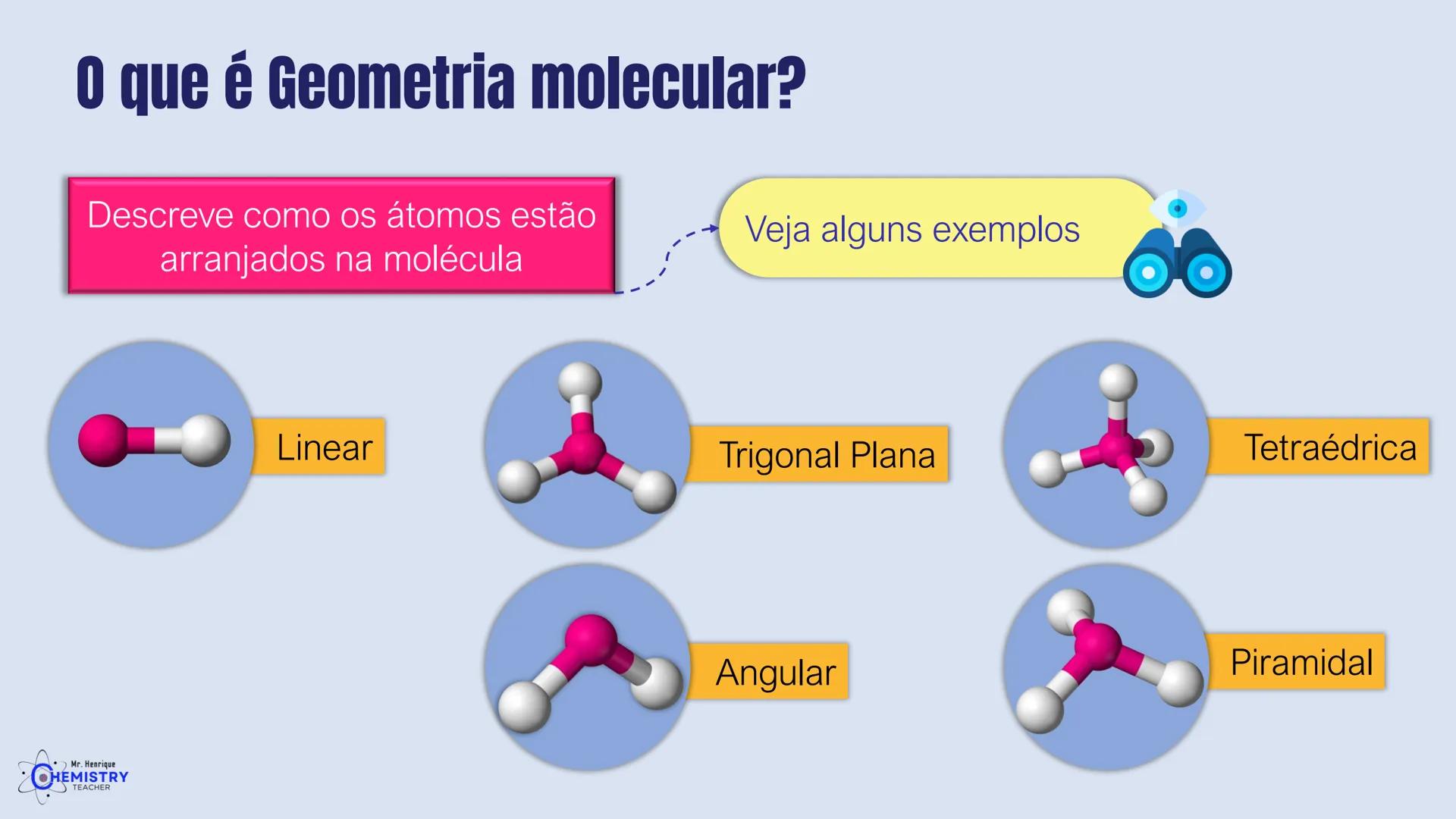
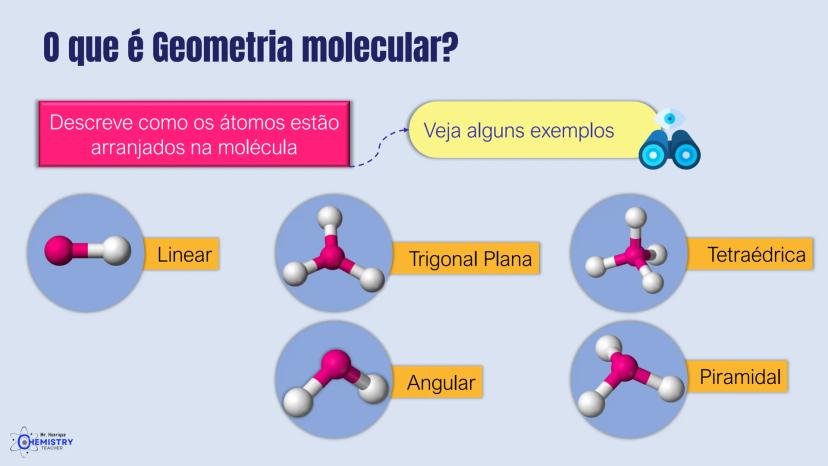
A geometria molecular simplesmente descreve como os átomos estão arranjados na molécula. É como se fosse a "arquitetura" das substâncias que determina sua forma no espaço tridimensional.
Existem vários tipos de geometrias moleculares que você precisa conhecer:
Cada uma dessas geometrias surge de um arranjo específico de átomos e suas ligações. A forma da molécula determina como ela interage com outras moléculas, afetando propriedades como solubilidade, ponto de ebulição e reatividade química.
🔍 Visualizar moléculas em 3D é mais fácil usando modelos! Você pode fazer isso com simulações digitais ou até mesmo com bolas e palitos para entender melhor.
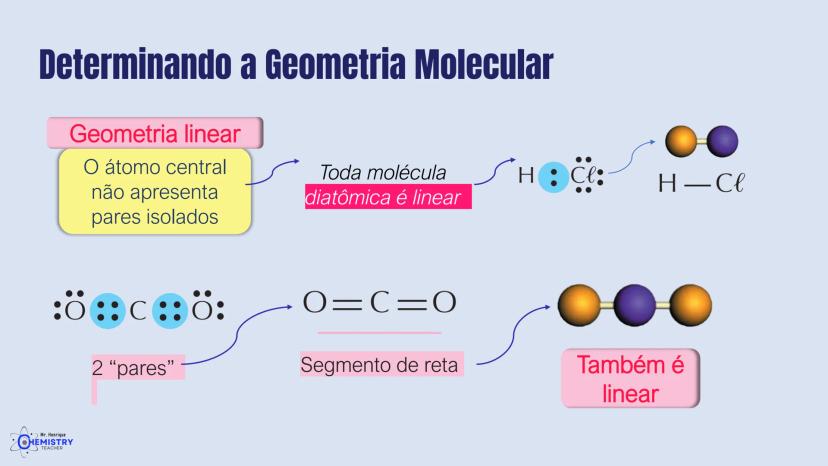
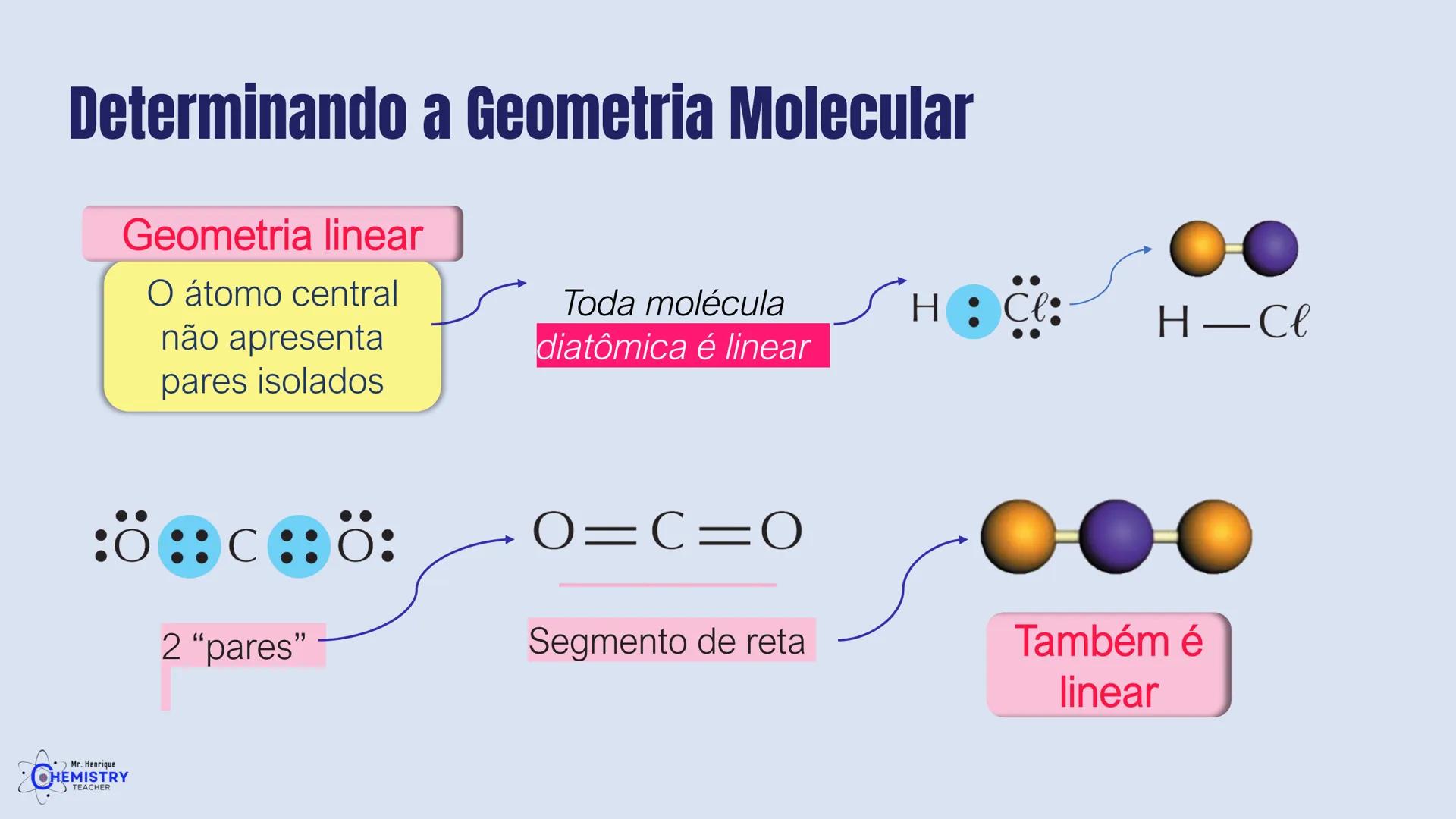
A geometria linear é uma das mais simples de identificar. Ela ocorre quando o átomo central não apresenta pares de elétrons isolados e forma ligações com apenas dois átomos ligantes.
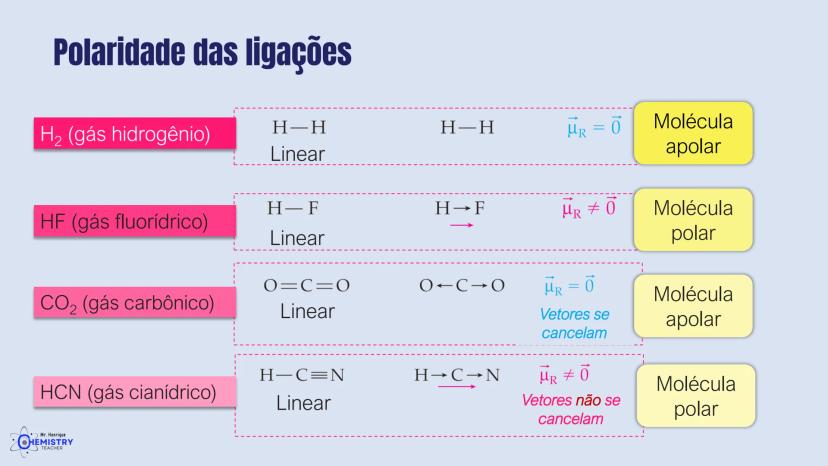
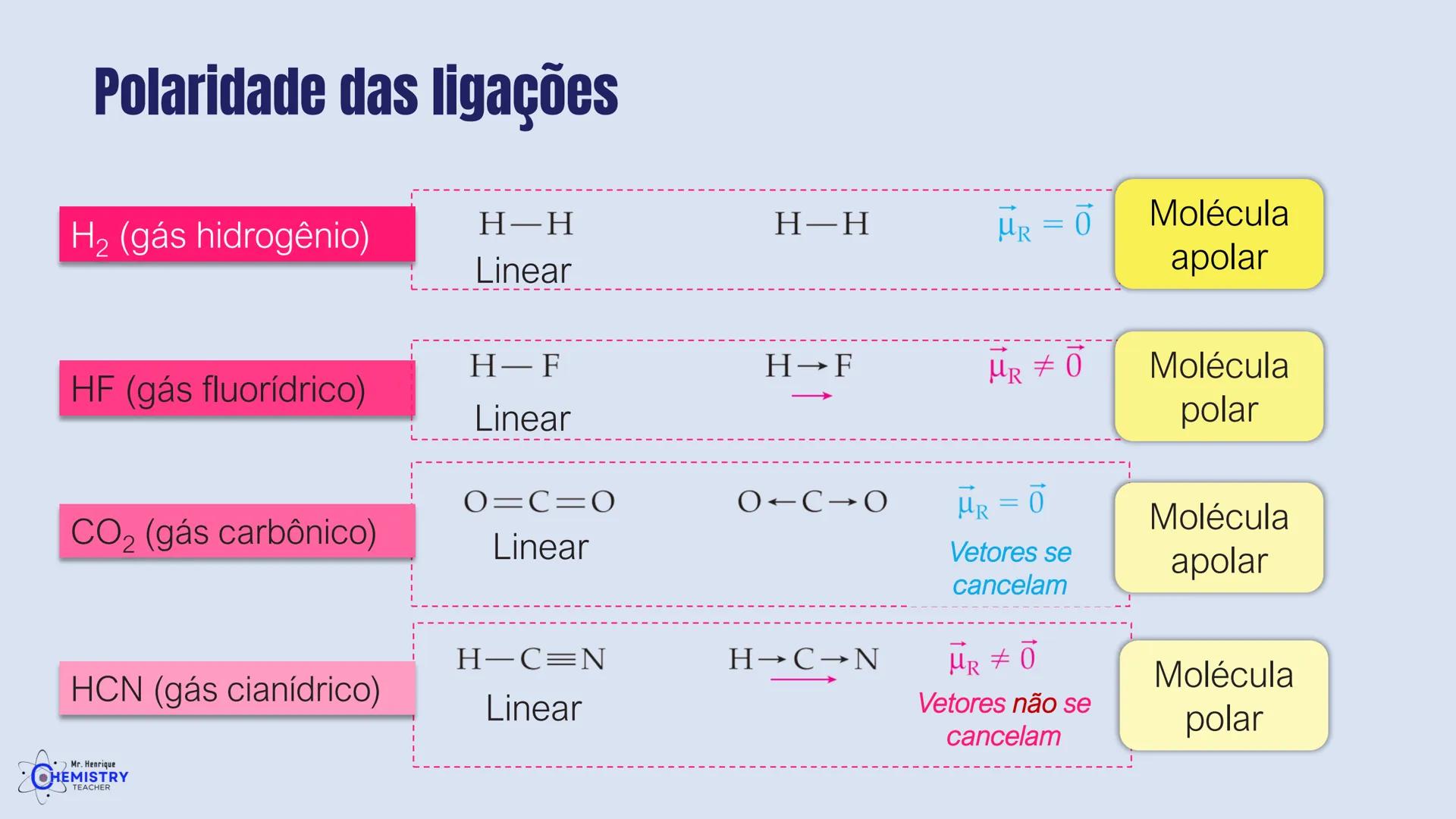
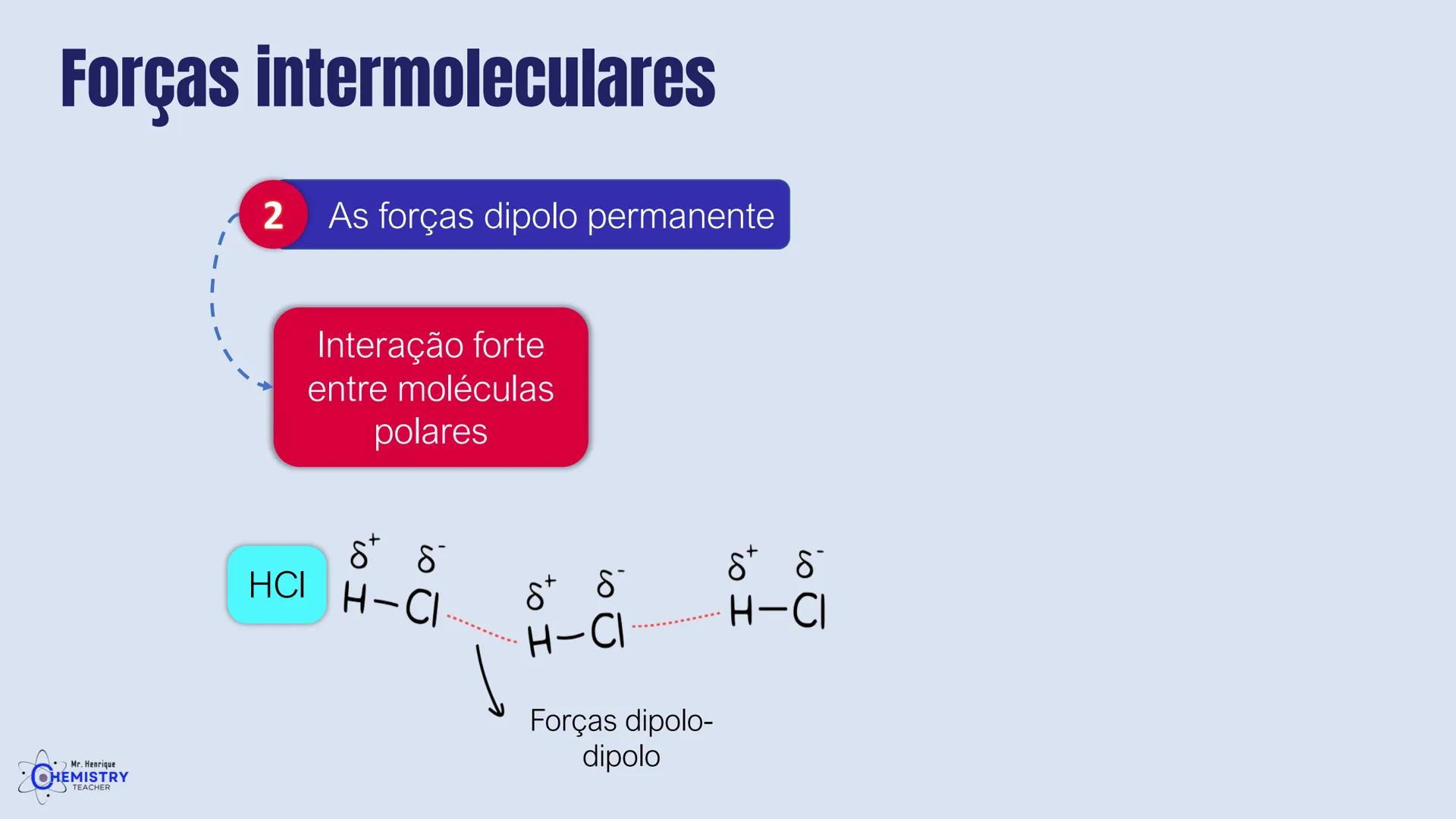
Toda molécula diatômica (formada por apenas dois átomos) é linear por natureza. Um exemplo clássico é o HCl (ácido clorídrico), onde o hidrogênio e o cloro estão ligados em linha reta: H-Cl.
Outro exemplo importante é o CO₂ (dióxido de carbono), que possui geometria linear com os átomos arranjados como O=C=O. Neste caso, o carbono (átomo central) forma duas ligações duplas com os átomos de oxigênio, criando um segmento de reta.
Esta geometria aparece quando os átomos ligados ao átomo central precisam ficar o mais distante possível uns dos outros, resultando em um ângulo de 180° entre as ligações.
💡 Lembre-se: na geometria linear, os átomos ficam a 180° um do outro, formando uma linha reta perfeita!
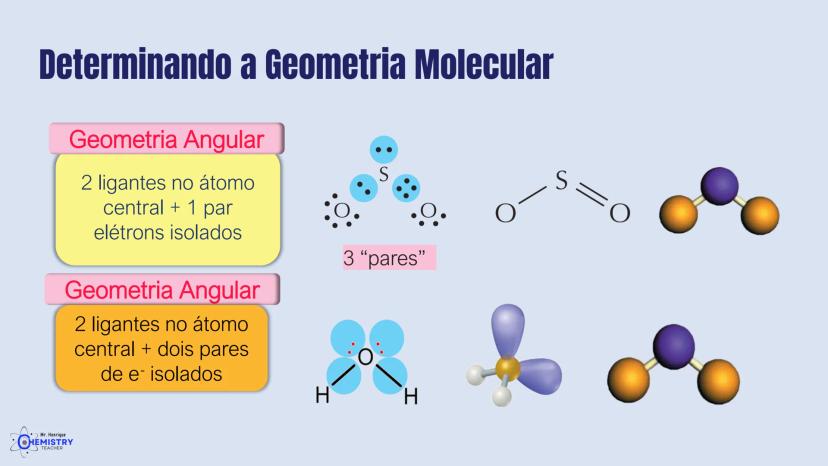
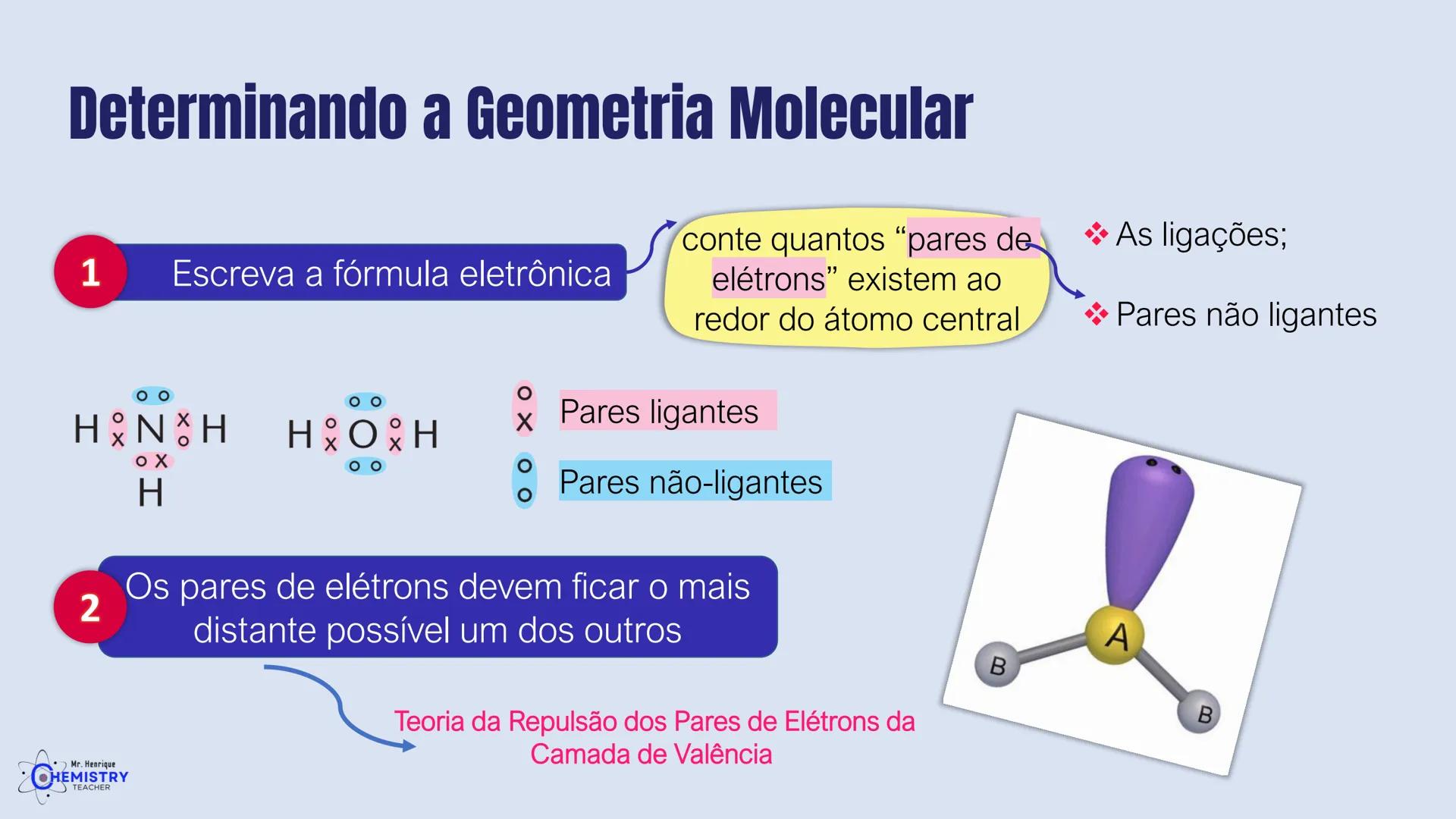
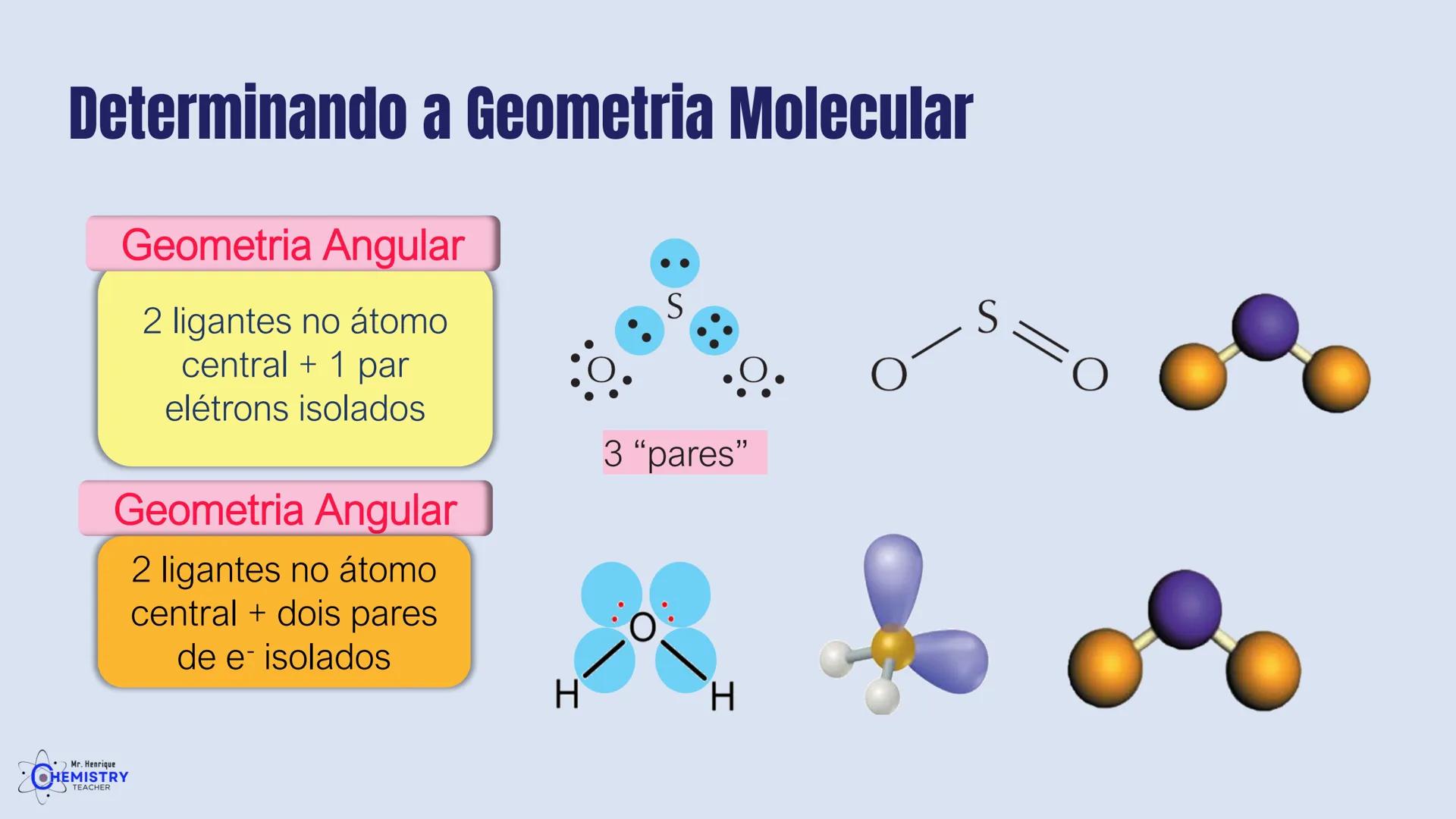
A geometria angular acontece em dois casos principais, ambos envolvendo pares de elétrons isolados (não ligantes) no átomo central.
No primeiro caso, temos a molécula com dois ligantes e um par de elétrons isolados no átomo central. A presença desse par isolado "empurra" os ligantes para mais perto um do outro, formando um ângulo menor que 180°.
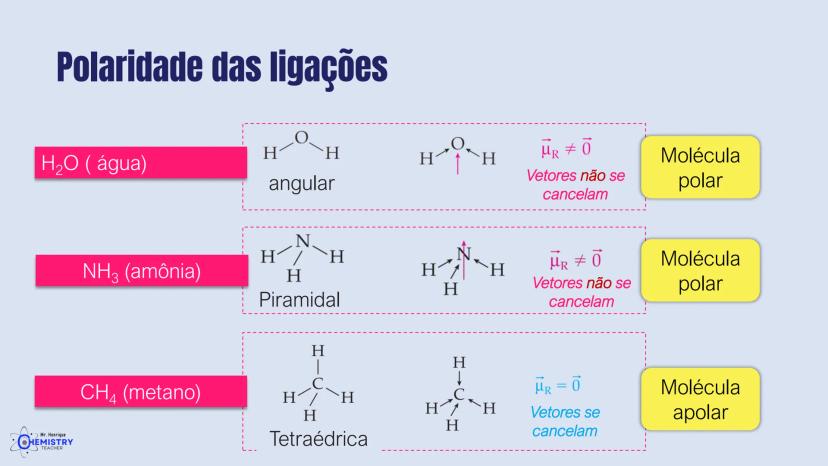
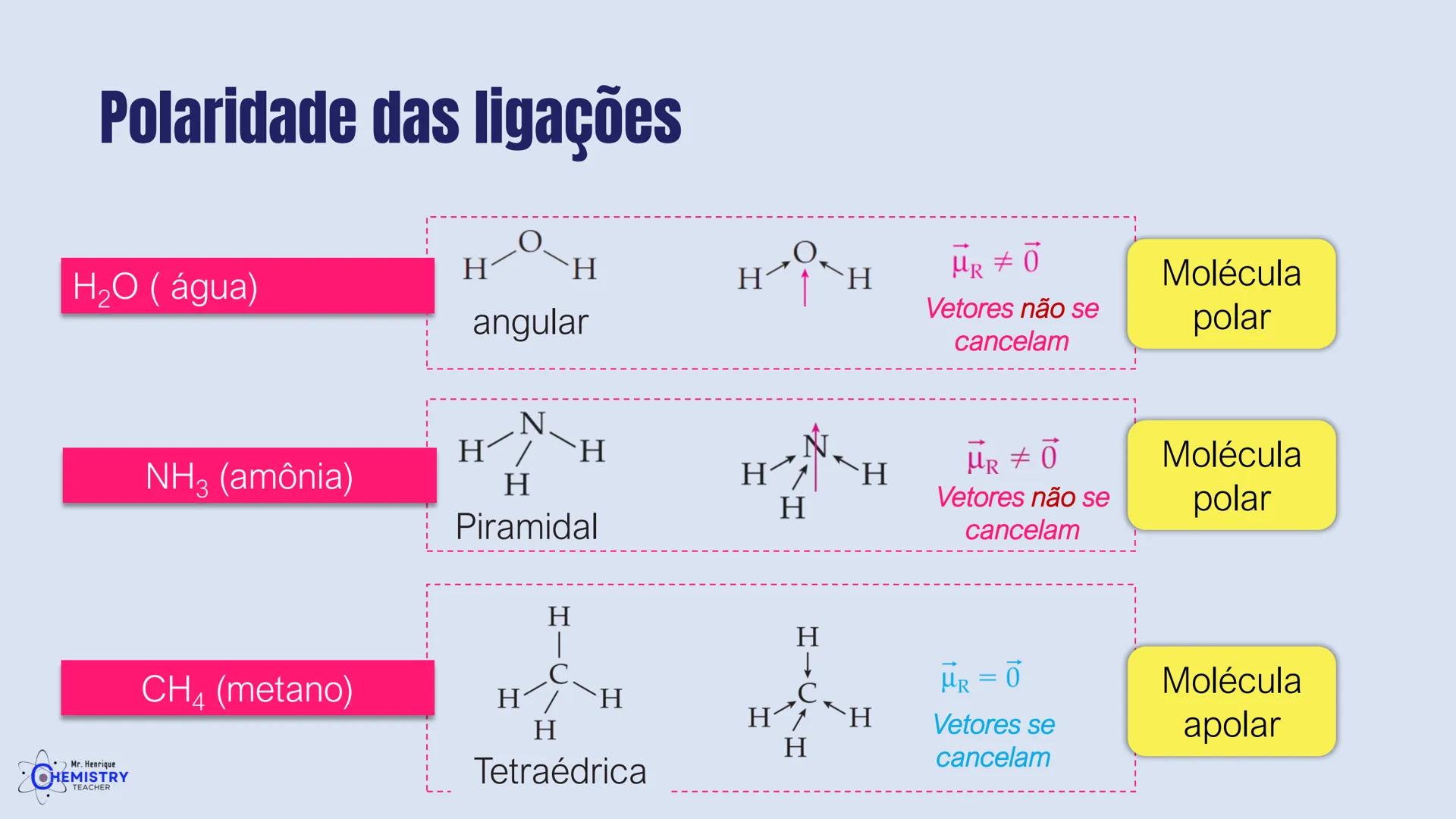
No segundo caso, quando temos dois ligantes e dois pares de elétrons isolados no átomo central, como na molécula de água (H₂O), os ligantes são forçados a ficar ainda mais próximos. Os pares isolados ocupam mais espaço e "comprimem" o ângulo entre as ligações.
A molécula de H₂S (sulfeto de hidrogênio) é outro bom exemplo de geometria angular. O átomo de enxofre possui dois pares de elétrons não ligantes e dois ligantes (os átomos de hidrogênio), resultando em uma estrutura em forma de "V".
🌊 A água (H₂O) tem geometria angular! Isso explica muitas de suas propriedades únicas e é essencial para a vida na Terra.
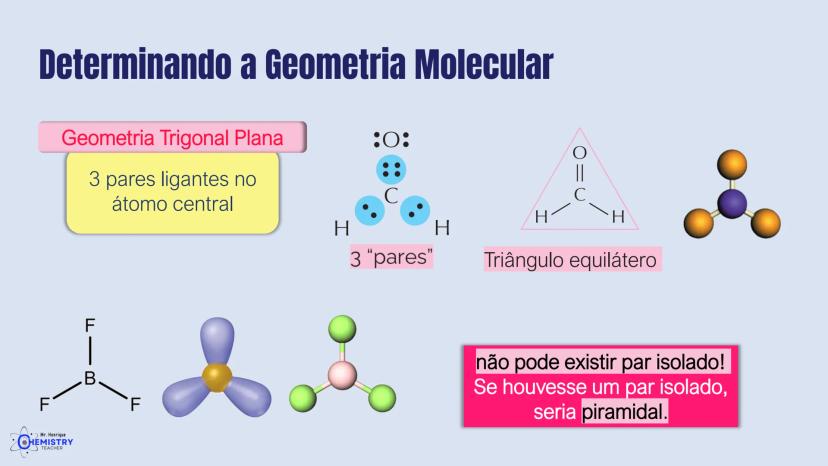
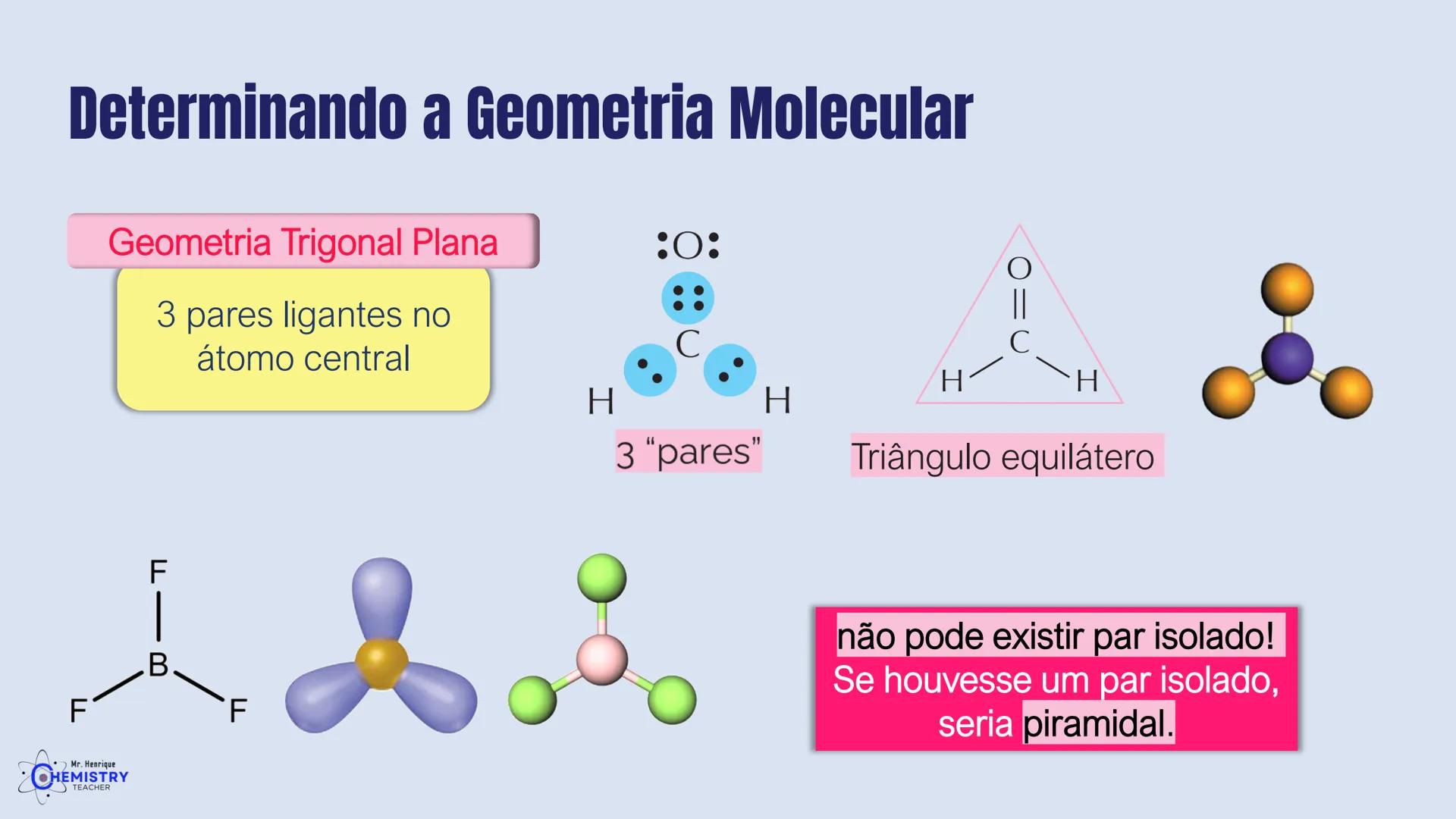
A geometria trigonal plana ocorre quando o átomo central forma três ligações com outros átomos e não possui pares de elétrons isolados. Os três átomos ligantes se organizam formando um triângulo equilátero, com ângulos de 120° entre si.
Um exemplo clássico é o BF₃ (trifluoreto de boro), onde o átomo de boro (B) está ligado a três átomos de flúor (F). Como não há pares isolados no boro, os átomos de flúor se distribuem no mesmo plano, o mais afastados possível uns dos outros.
Outro exemplo é a molécula de eteno (C₂H₄), onde cada átomo de carbono adota uma geometria trigonal plana em relação aos átomos a ele ligados.
É importante notar que se houvesse um par de elétrons isolado no átomo central, a geometria não seria mais trigonal plana, mas sim piramidal, pois o par isolado ocuparia uma das posições do espaço tridimensional.
🔺 Uma forma fácil de lembrar: na geometria trigonal plana, os átomos formam um triângulo perfeito no mesmo plano, sem nenhuma projeção para cima ou para baixo.
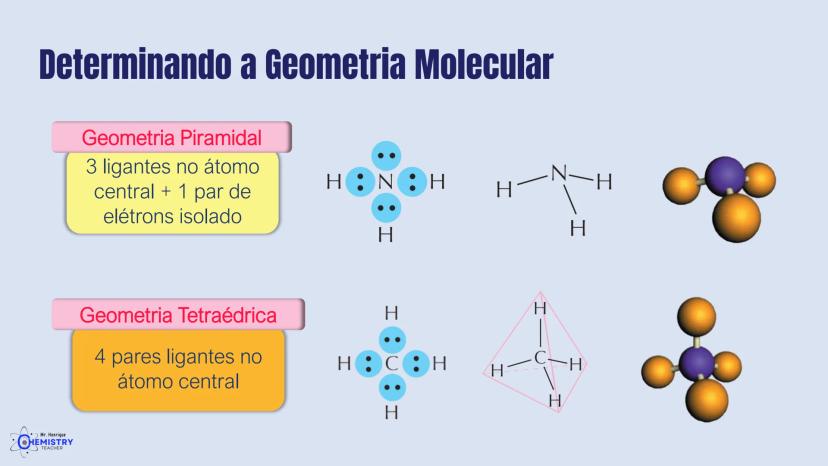
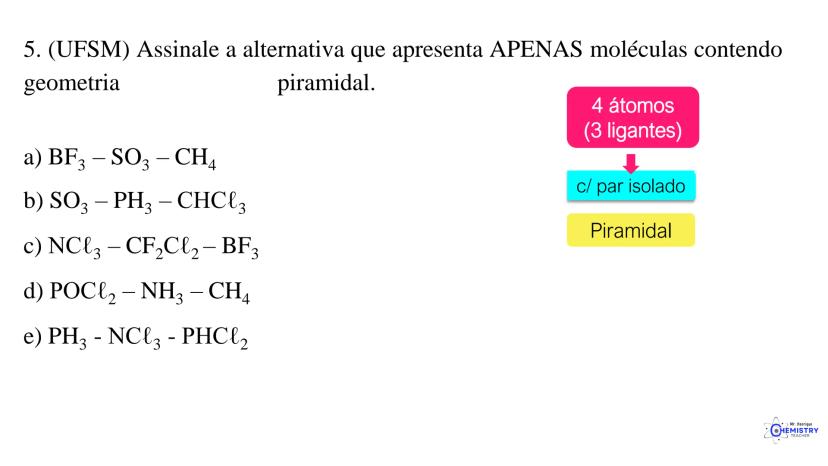
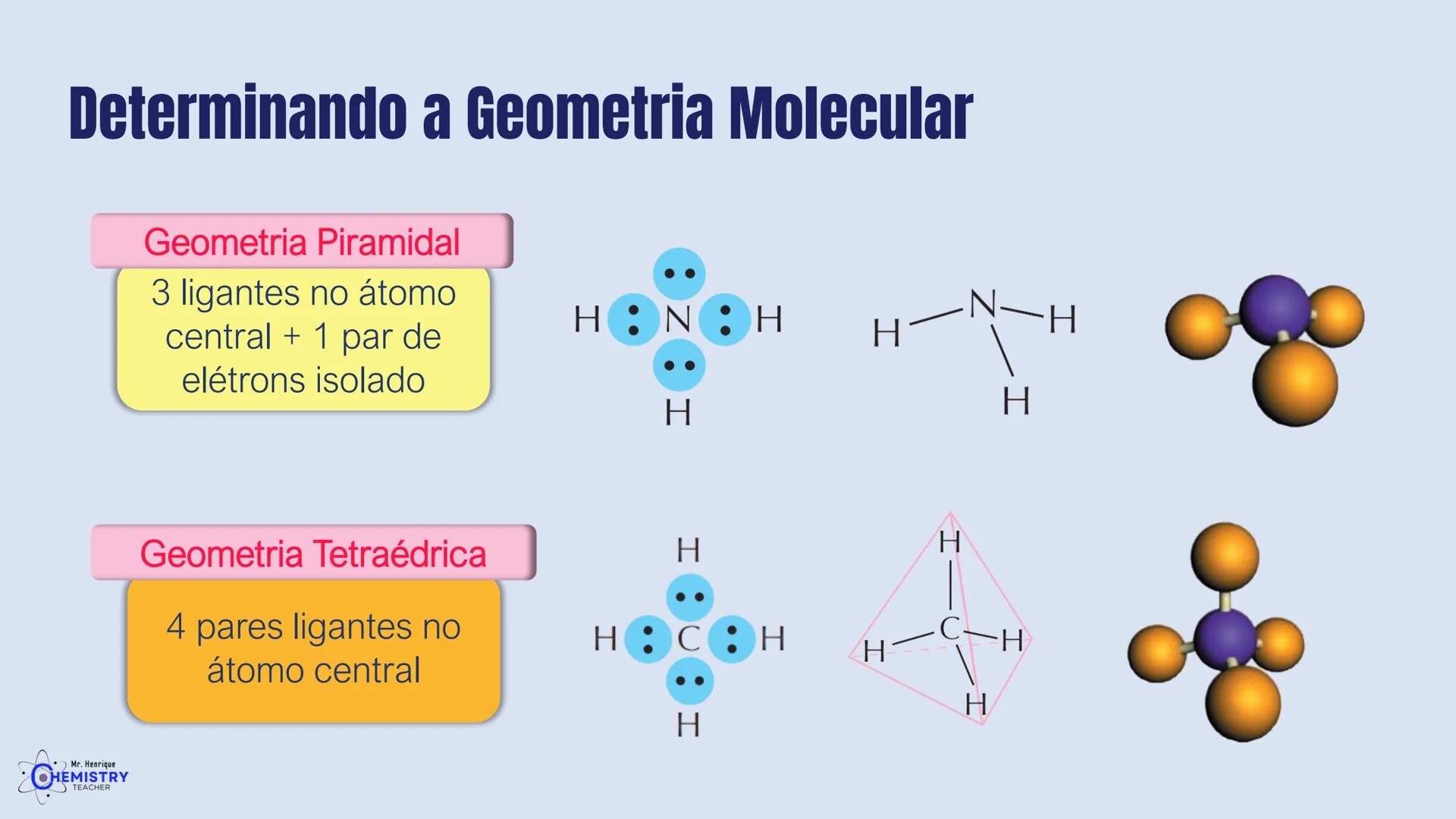
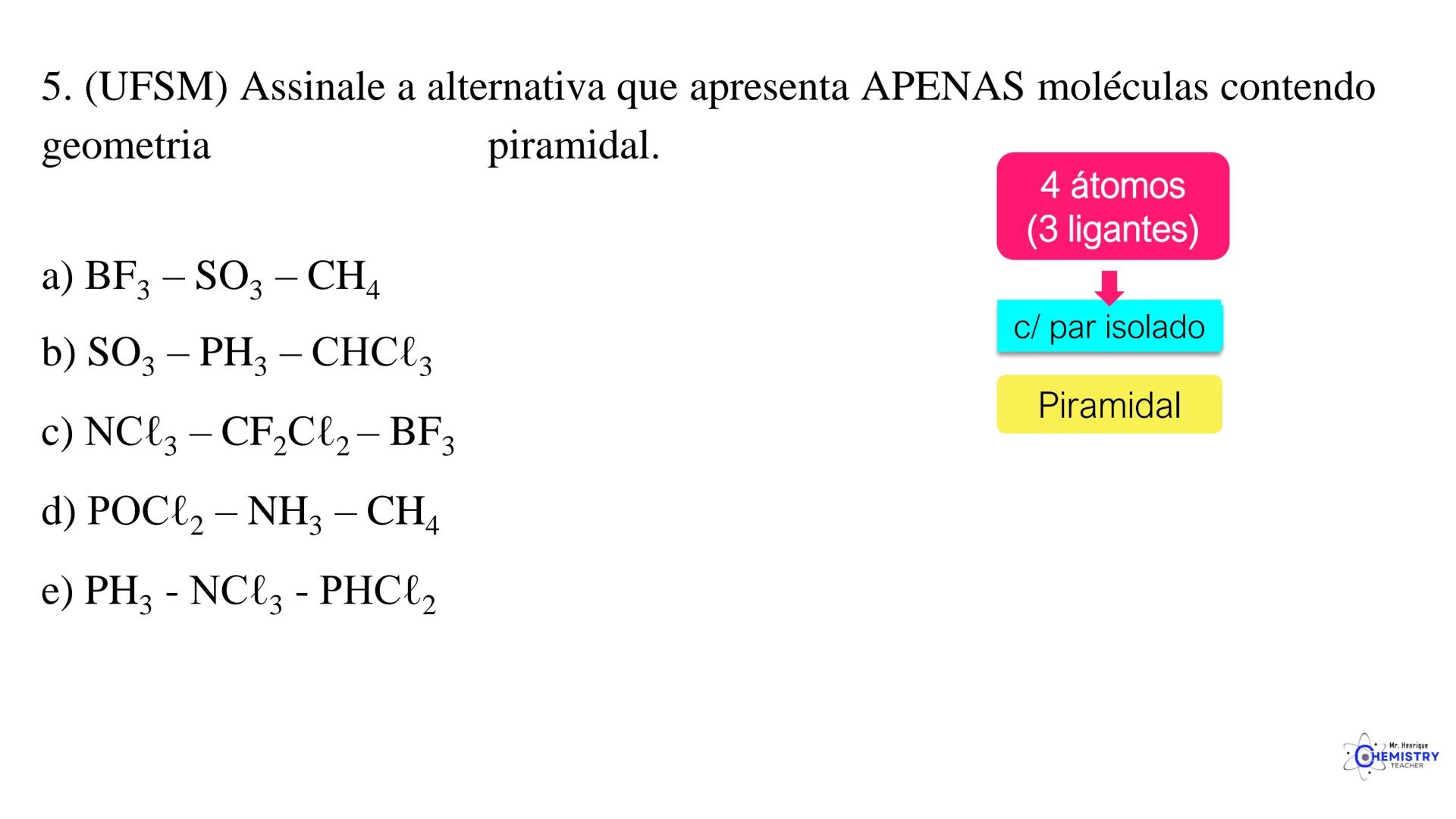
A geometria piramidal ocorre quando o átomo central possui três ligantes e um par de elétrons isolados. Esse arranjo forma uma estrutura semelhante a uma pirâmide, com o átomo central no topo e os três ligantes formando a base.
Um exemplo clássico é a molécula de amônia (NH₃), onde o átomo de nitrogênio possui três ligações com hidrogênios e um par de elétrons isolados. O par isolado "empurra" os hidrogênios para baixo, criando a forma piramidal.
Já a geometria tetraédrica aparece quando o átomo central forma quatro ligações (tem quatro pares ligantes) e não possui pares isolados. Os quatro átomos ligantes se posicionam nos vértices de um tetraedro imaginário.
O exemplo mais conhecido é o metano (CH₄), onde o carbono está ligado a quatro átomos de hidrogênio. Os hidrogênios se posicionam o mais distante possível uns dos outros, formando um tetraedro perfeito com ângulos de aproximadamente 109,5° entre as ligações.
💎 Visualize um tetraedro como uma pirâmide de base triangular. Na geometria tetraédrica, o átomo central fica no meio e os quatro ligantes ficam nos vértices.
Para moléculas mais complexas, temos geometrias que acomodam mais ligantes ao redor do átomo central.
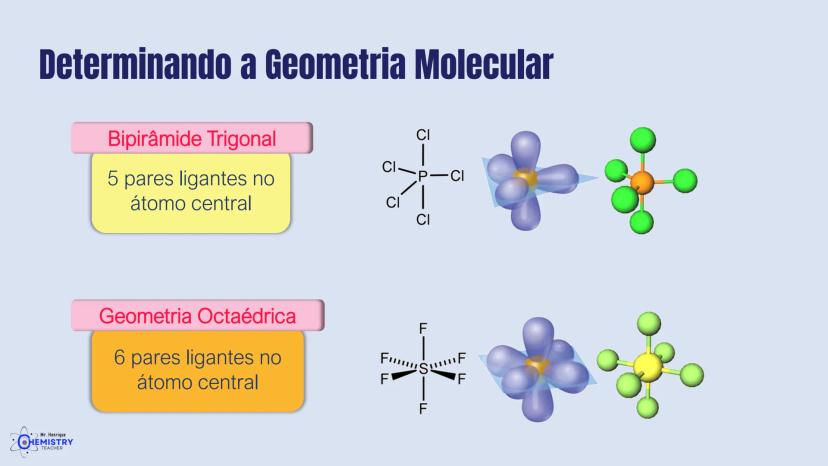
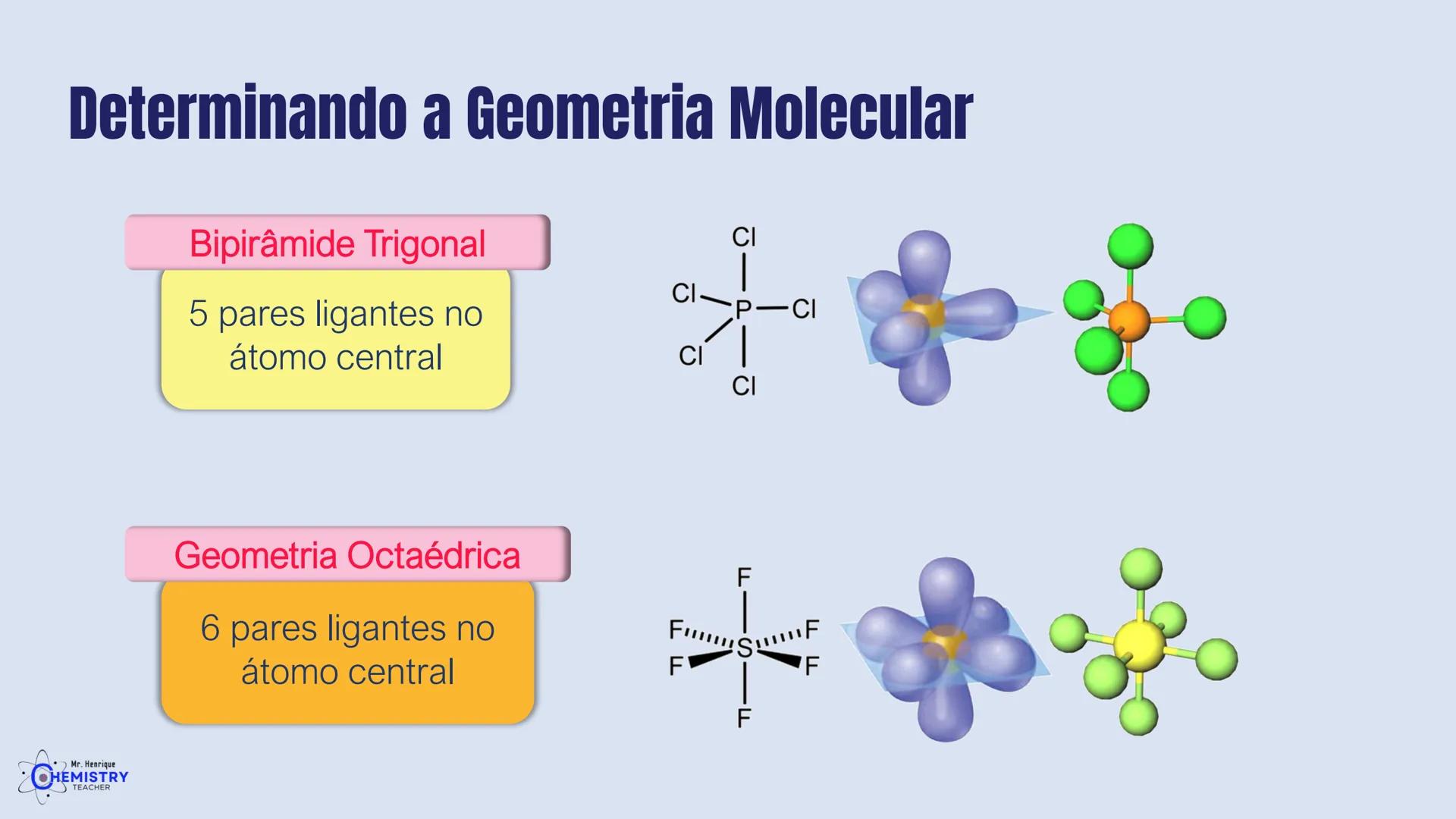
A geometria de bipirâmide trigonal acontece quando o átomo central forma cinco ligações (tem cinco pares ligantes). Nesta configuração, três átomos ficam no mesmo plano formando um triângulo equilátero (como na geometria trigonal plana), e os outros dois ficam acima e abaixo desse plano, formando os "polos" da bipirâmide.
Um exemplo desta geometria é o PCl₅ (pentacloreto de fósforo), onde o átomo de fósforo está ligado a cinco átomos de cloro.
A geometria octaédrica ocorre quando o átomo central forma seis ligações (tem seis pares ligantes). Neste caso, os ligantes se posicionam nos vértices de um octaedro, que pode ser visualizado como dois quadrados superpostos e rotacionados 45° um em relação ao outro.
Um exemplo é o SF₆ (hexafluoreto de enxofre), onde o enxofre está ligado a seis átomos de flúor em uma disposição octaédrica.
🧩 Estas geometrias moleculares mais complexas são importantes em compostos usados em medicamentos, catalisadores e materiais avançados.
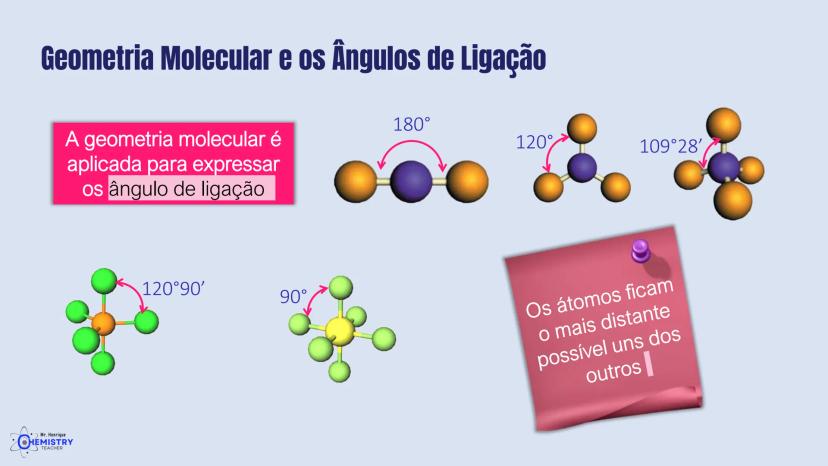
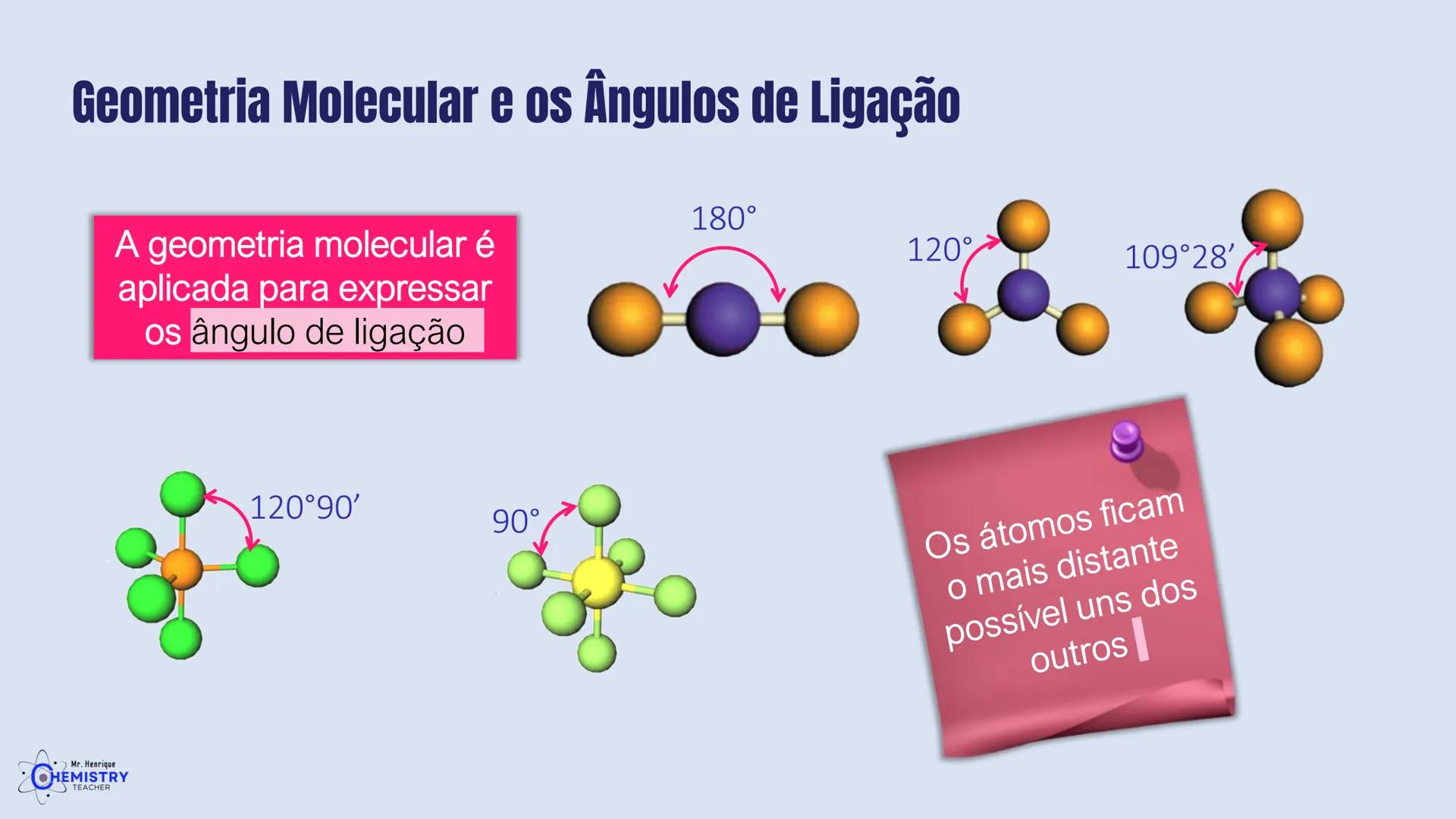
Os ângulos entre as ligações são uma consequência direta da geometria molecular. Eles expressam numericamente como os átomos estão organizados no espaço tridimensional.
Cada geometria tem seus ângulos característicos:
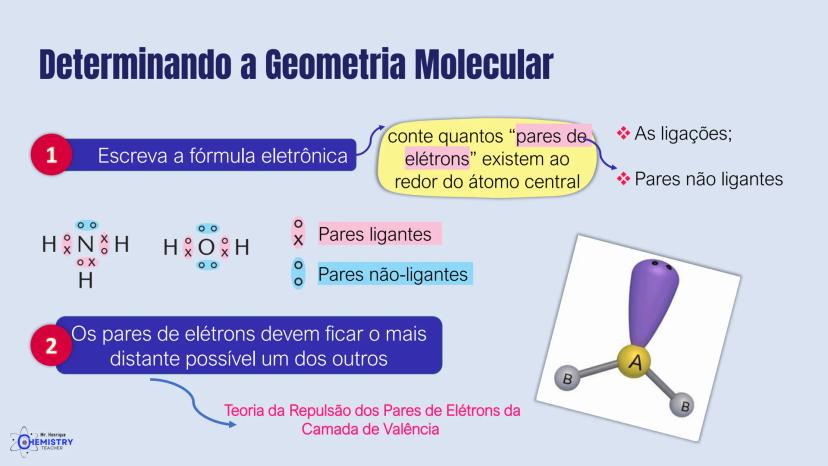
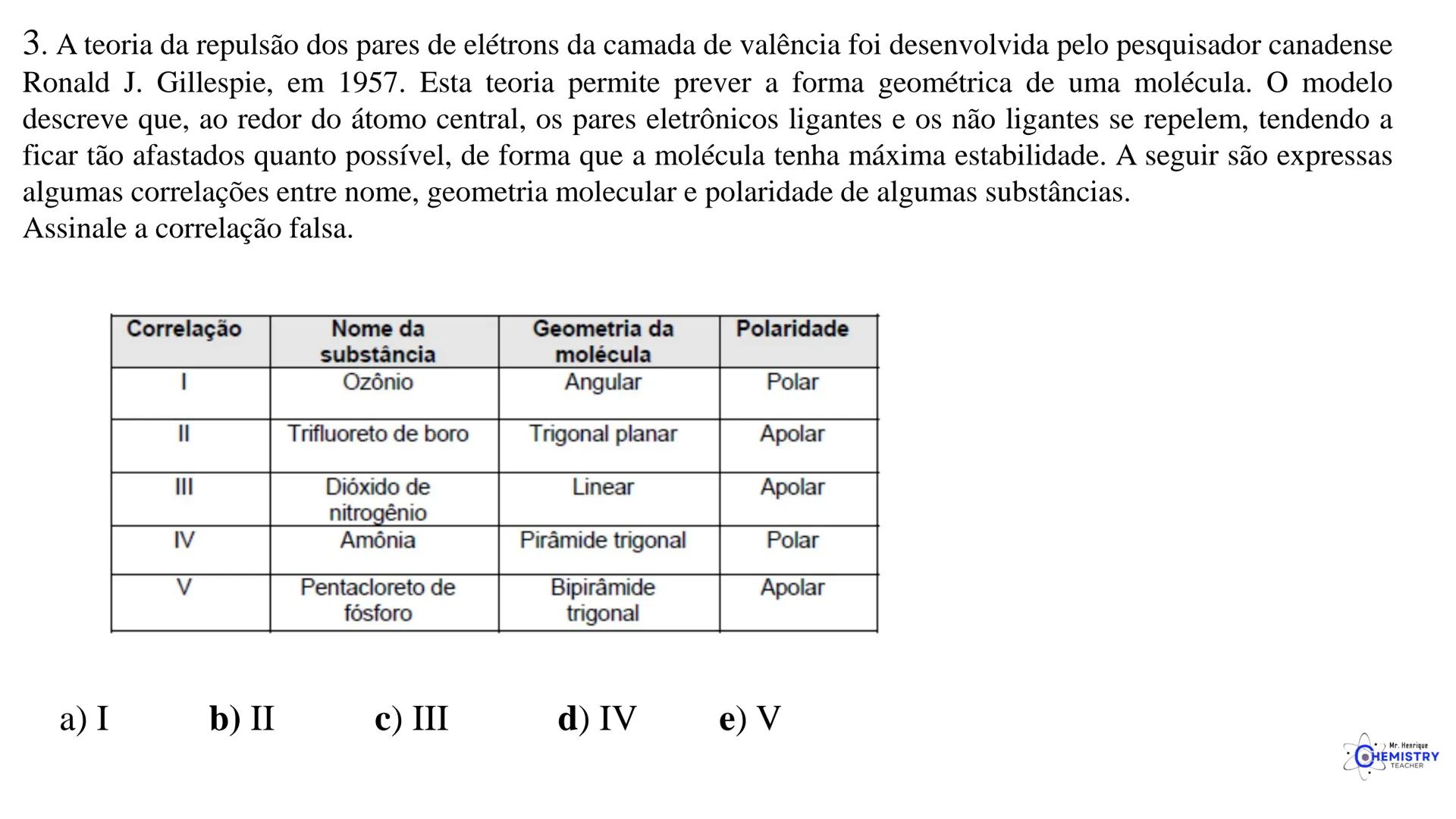
Esses ângulos ocorrem porque os átomos e os pares de elétrons tendem a se posicionar o mais distante possível uns dos outros. Esta é a base da Teoria da Repulsão dos Pares de Elétrons da Camada de Valência (VSEPR), que explica a geometria das moléculas.
Os pares isolados (não ligantes) exercem uma repulsão maior que os pares ligantes, o que pode alterar ligeiramente os ângulos ideais. Por exemplo, na água (H₂O), o ângulo é aproximadamente 104,5° em vez dos 109,5° de uma tetraédrica perfeita.
🧭 Os ângulos de ligação são como uma bússola para entender a estrutura molecular. Eles nos ajudam a prever como a molécula interage com outras substâncias.
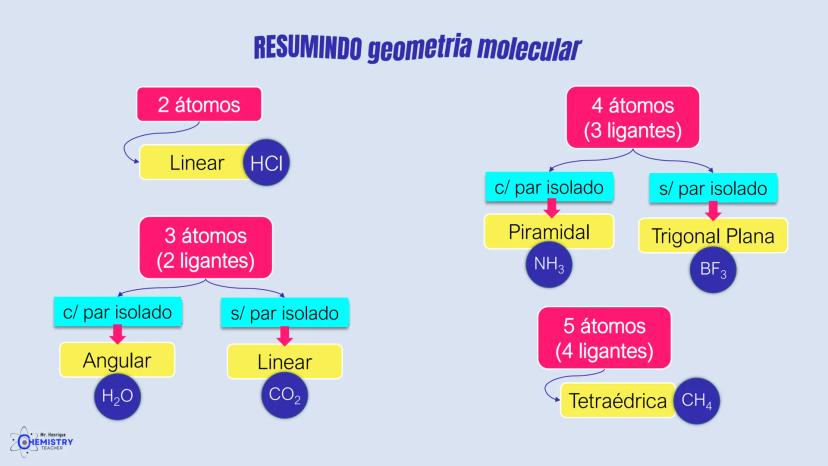
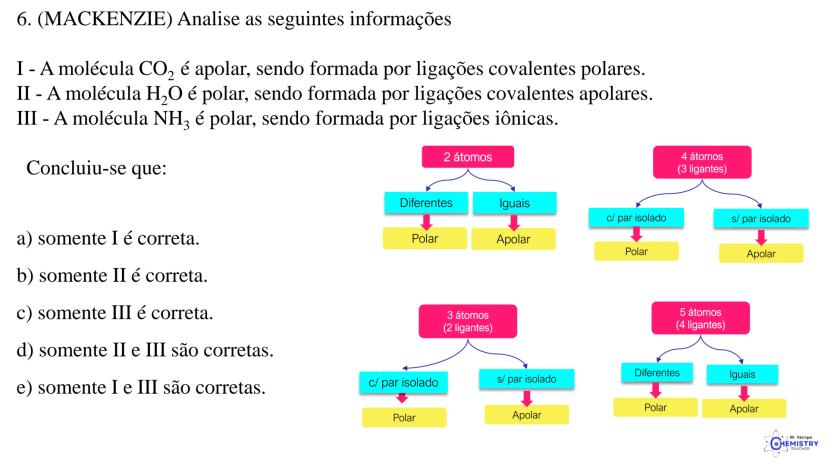
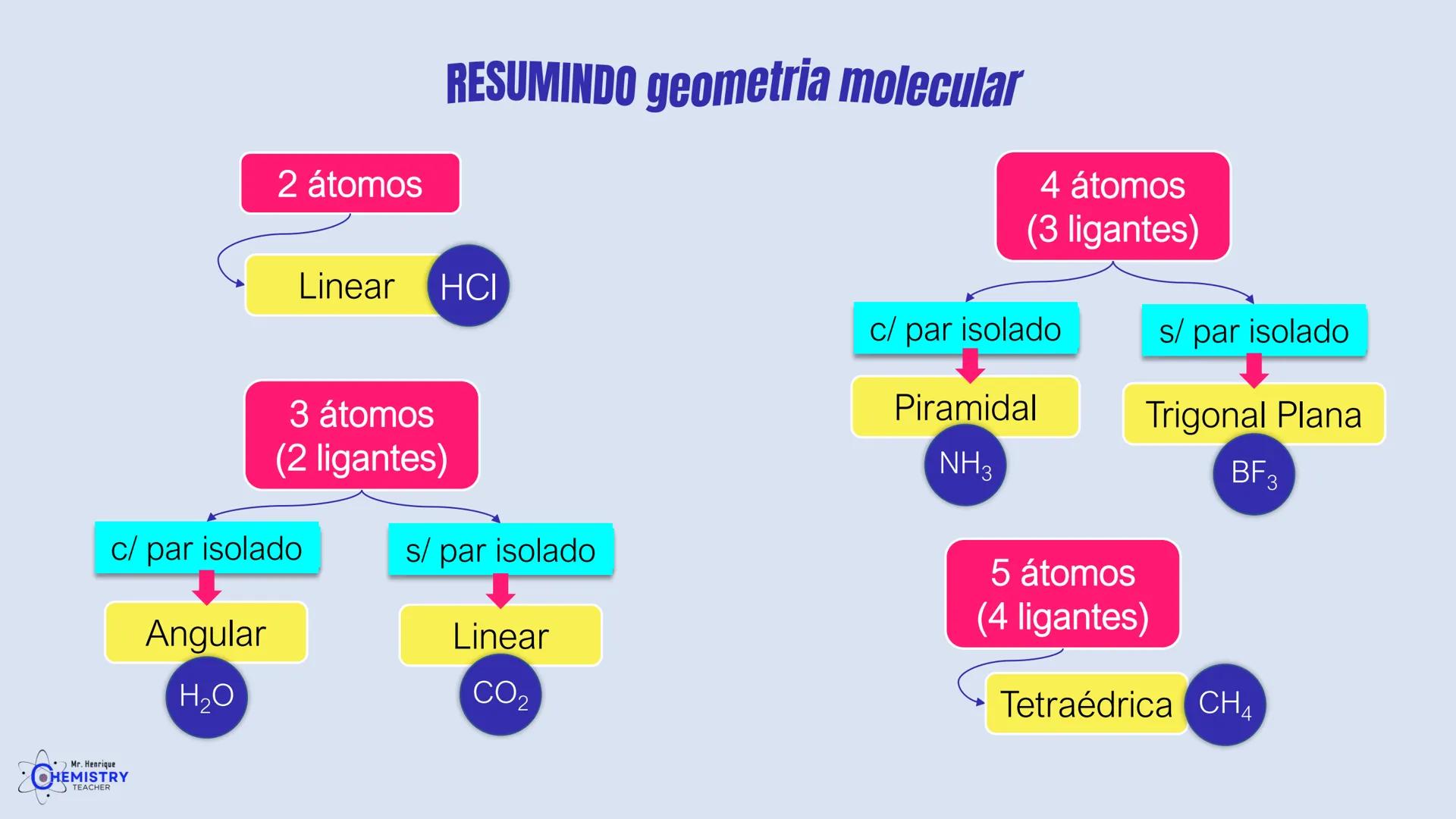
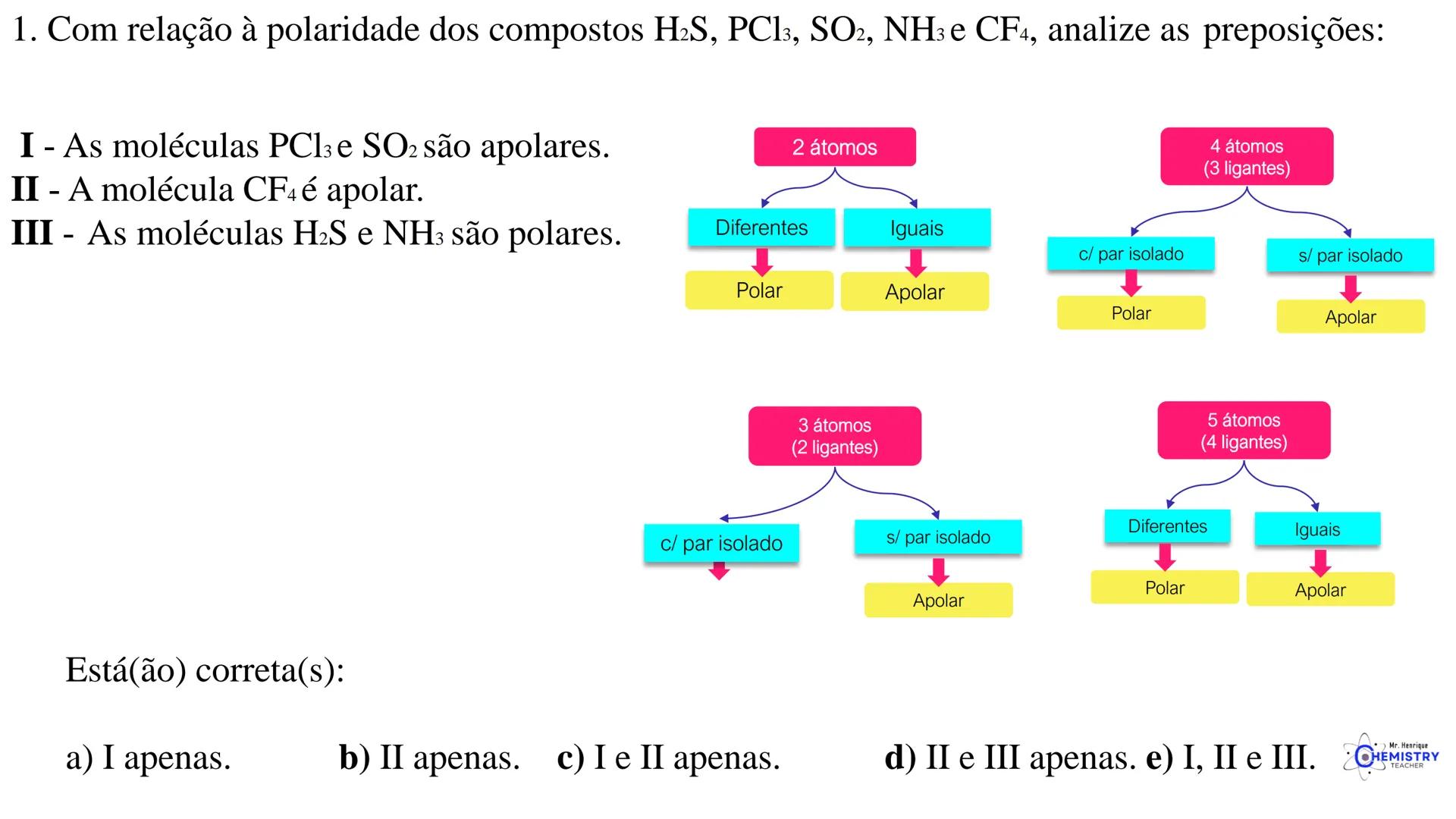
Vamos organizar o que aprendemos sobre geometria molecular de forma prática:
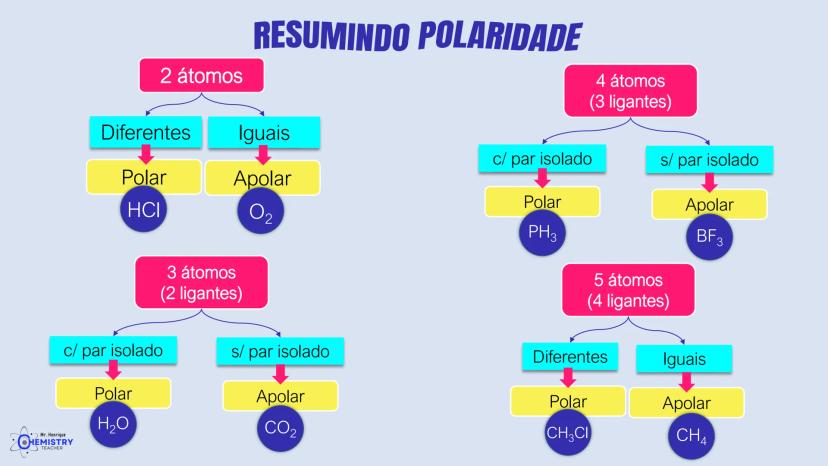
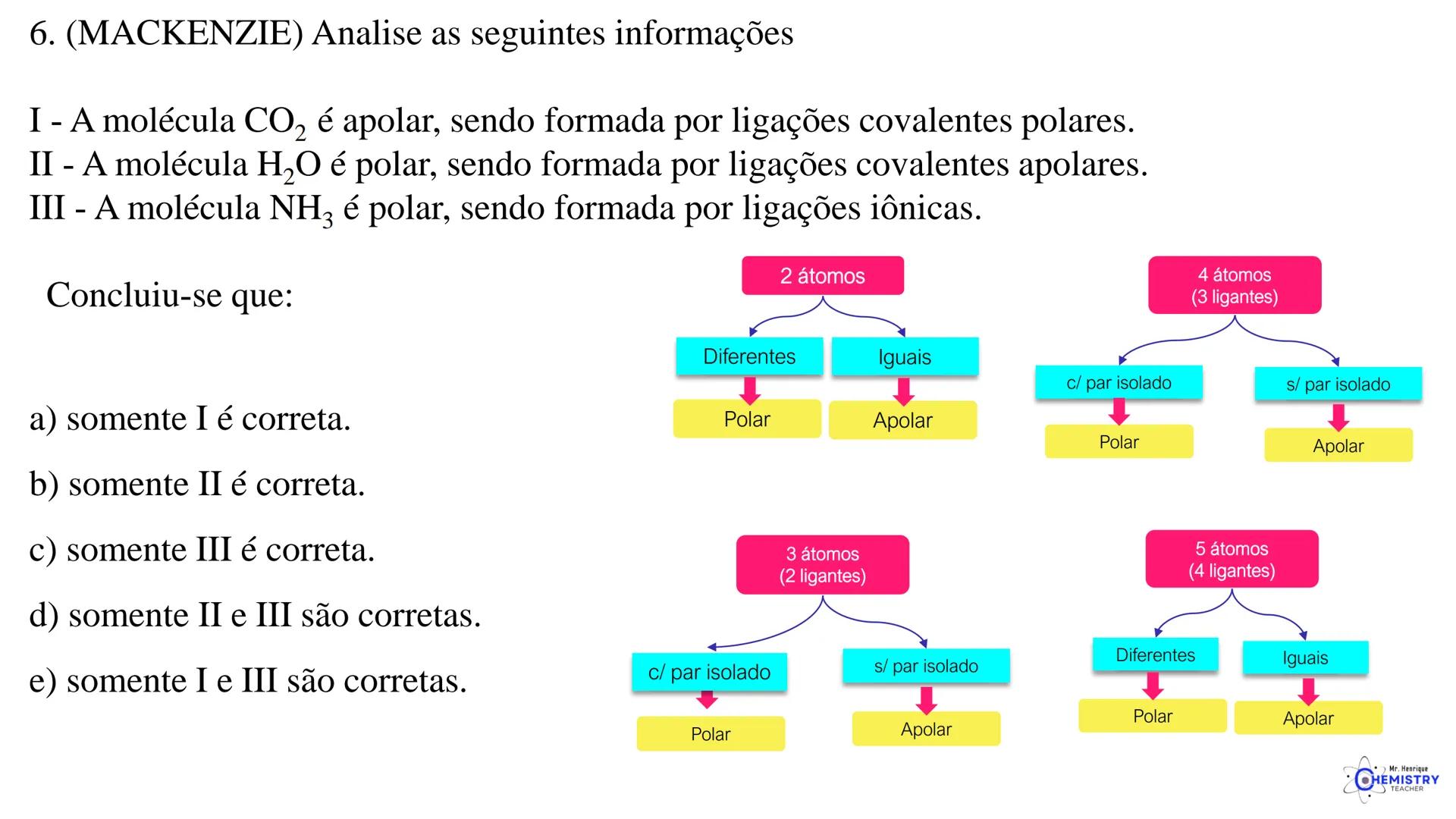
Para moléculas com 2 átomos:
Para moléculas com 3 átomos (2 ligantes no átomo central):
Para moléculas com 4 átomos (3 ligantes no átomo central):
Para moléculas com 5 átomos (4 ligantes no átomo central):
A chave para determinar a geometria molecular é contar tanto os átomos ligantes quanto os pares de elétrons isolados ao redor do átomo central, e entender como eles se repelem entre si.
📏 Uma dica para facilitar: conte primeiro o número total de pares de elétrons ao redor do átomo central para determinar a "geometria eletrônica", depois veja quantos desses pares são realmente ligantes para determinar a geometria molecular.
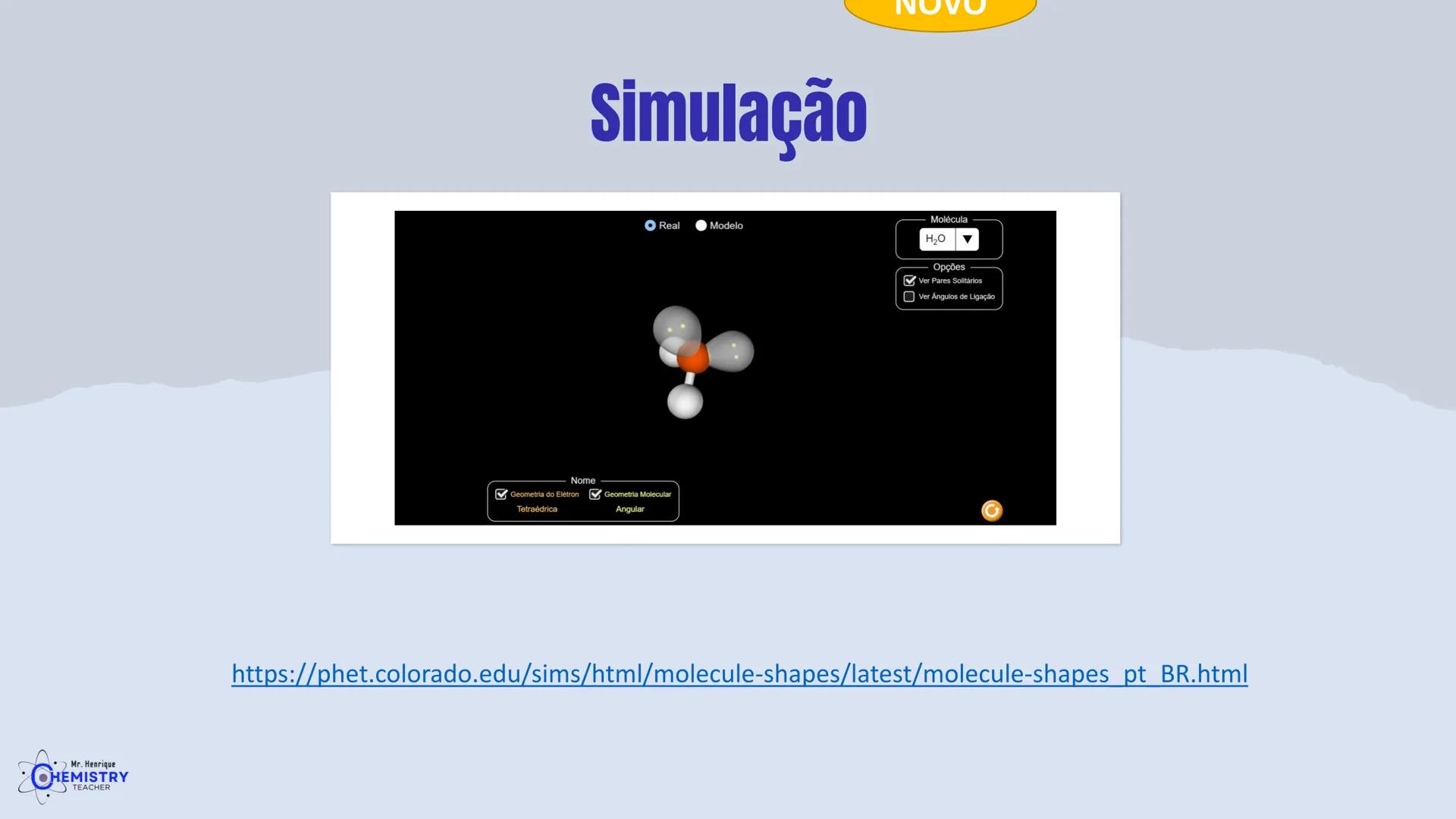
As simulações computacionais são ferramentas poderosas para visualizar e compreender a geometria molecular. Elas permitem que você veja as moléculas em três dimensões e entenda como os átomos estão arranjados no espaço.
A simulação PhET do Colorado é um recurso excelente que permite:
Estas ferramentas interativas ajudam a compreender como a repulsão entre os pares de elétrons determina a forma das moléculas. Você pode, por exemplo, adicionar ou remover ligantes e pares isolados para ver como a geometria se altera.
Ao explorar moléculas como a água (H₂O) na simulação, você pode observar sua geometria angular e entender por que esse arranjo é crucial para as propriedades únicas da água.
💻 Experimente a simulação! É uma maneira divertida e interativa de aprender sobre geometria molecular - muito melhor que apenas ler sobre isso no livro.







Nosso companheiro de IA foi criado especificamente para atender às necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos oferecer respostas realmente relevantes e significativas. Mas não se trata apenas de respostas, o companheiro também está aqui para guiar você pelos desafios diários de aprendizado, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização com base nas suas habilidades e desenvolvimentos.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
App Store
Google Play
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
Sophia Lima Sophia
@sophialimasophi
A geometria molecular e as forças intermoleculares são temas fascinantes que explicam como os átomos se organizam nas moléculas e como estas interagem entre si. Esses conceitos são fundamentais para entender diversas propriedades físicas e químicas das substâncias que nos... Mostrar mais

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A química do 9º ano nos apresenta um tema super importante: como as moléculas se organizam no espaço! A geometria molecular descreve o arranjo tridimensional dos átomos e influencia diretamente as propriedades das substâncias.
Você já parou para pensar por que algumas substâncias se dissolvem em água e outras não? Ou por que alguns gases têm pontos de ebulição tão diferentes? A resposta está na geometria das moléculas e na sua polaridade.
Neste estudo, vamos descobrir como prever as formas das moléculas e entender como essas formas afetam o comportamento das substâncias no mundo real.
💡 Saber a geometria molecular não é apenas decorar formas! É entender como a natureza organiza os átomos para criar todas as substâncias que conhecemos.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A geometria molecular simplesmente descreve como os átomos estão arranjados na molécula. É como se fosse a "arquitetura" das substâncias que determina sua forma no espaço tridimensional.
Existem vários tipos de geometrias moleculares que você precisa conhecer:
Cada uma dessas geometrias surge de um arranjo específico de átomos e suas ligações. A forma da molécula determina como ela interage com outras moléculas, afetando propriedades como solubilidade, ponto de ebulição e reatividade química.
🔍 Visualizar moléculas em 3D é mais fácil usando modelos! Você pode fazer isso com simulações digitais ou até mesmo com bolas e palitos para entender melhor.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A geometria linear é uma das mais simples de identificar. Ela ocorre quando o átomo central não apresenta pares de elétrons isolados e forma ligações com apenas dois átomos ligantes.
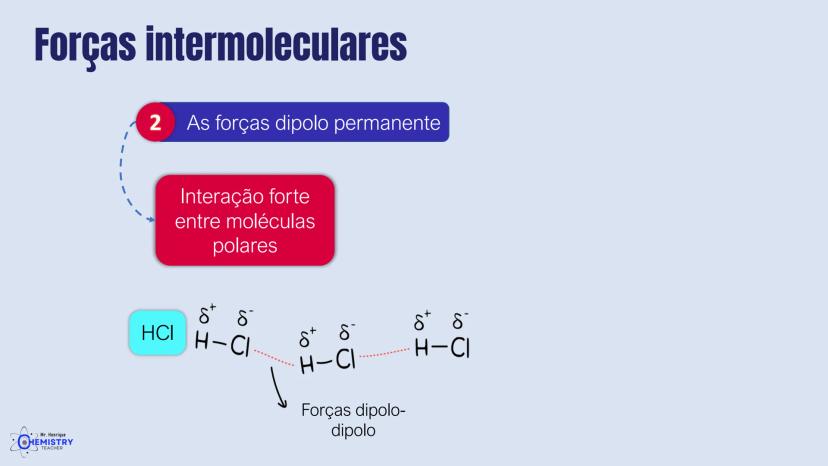
Toda molécula diatômica (formada por apenas dois átomos) é linear por natureza. Um exemplo clássico é o HCl (ácido clorídrico), onde o hidrogênio e o cloro estão ligados em linha reta: H-Cl.
Outro exemplo importante é o CO₂ (dióxido de carbono), que possui geometria linear com os átomos arranjados como O=C=O. Neste caso, o carbono (átomo central) forma duas ligações duplas com os átomos de oxigênio, criando um segmento de reta.
Esta geometria aparece quando os átomos ligados ao átomo central precisam ficar o mais distante possível uns dos outros, resultando em um ângulo de 180° entre as ligações.
💡 Lembre-se: na geometria linear, os átomos ficam a 180° um do outro, formando uma linha reta perfeita!

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A geometria angular acontece em dois casos principais, ambos envolvendo pares de elétrons isolados (não ligantes) no átomo central.
No primeiro caso, temos a molécula com dois ligantes e um par de elétrons isolados no átomo central. A presença desse par isolado "empurra" os ligantes para mais perto um do outro, formando um ângulo menor que 180°.
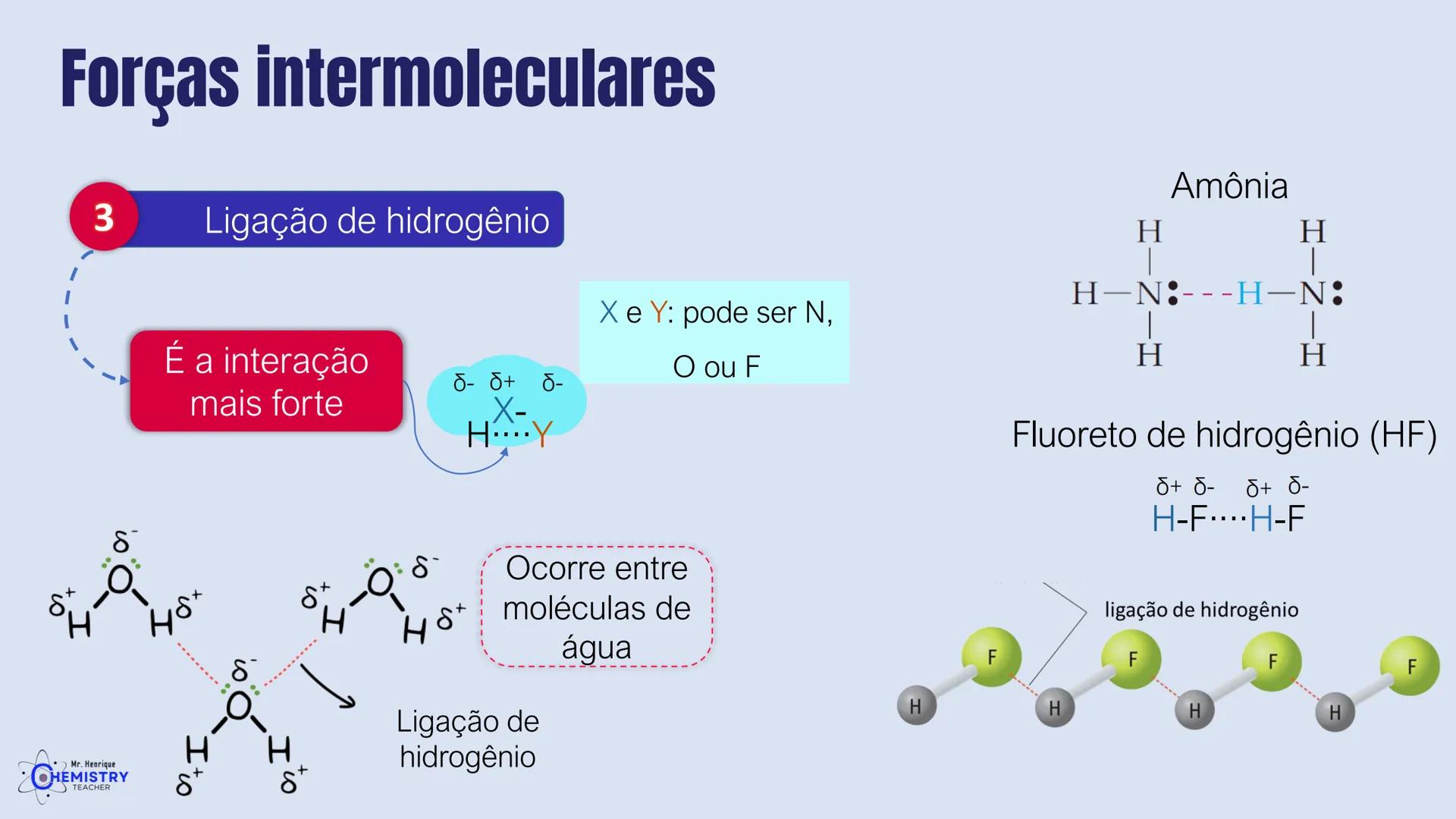
No segundo caso, quando temos dois ligantes e dois pares de elétrons isolados no átomo central, como na molécula de água (H₂O), os ligantes são forçados a ficar ainda mais próximos. Os pares isolados ocupam mais espaço e "comprimem" o ângulo entre as ligações.
A molécula de H₂S (sulfeto de hidrogênio) é outro bom exemplo de geometria angular. O átomo de enxofre possui dois pares de elétrons não ligantes e dois ligantes (os átomos de hidrogênio), resultando em uma estrutura em forma de "V".
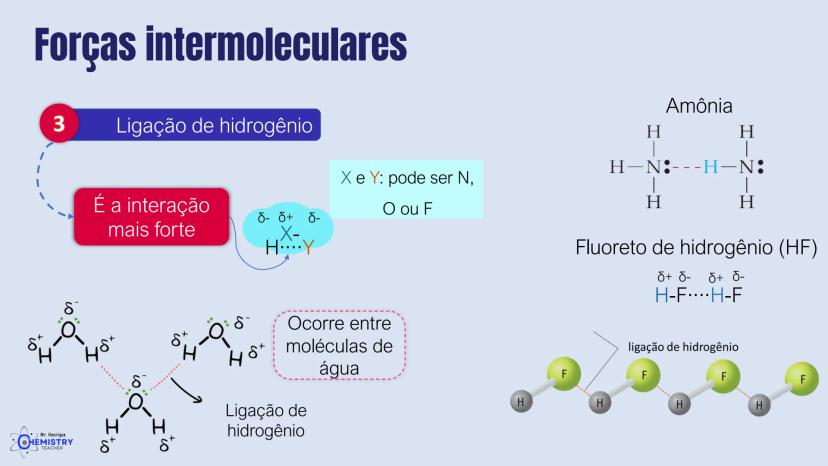
🌊 A água (H₂O) tem geometria angular! Isso explica muitas de suas propriedades únicas e é essencial para a vida na Terra.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A geometria trigonal plana ocorre quando o átomo central forma três ligações com outros átomos e não possui pares de elétrons isolados. Os três átomos ligantes se organizam formando um triângulo equilátero, com ângulos de 120° entre si.
Um exemplo clássico é o BF₃ (trifluoreto de boro), onde o átomo de boro (B) está ligado a três átomos de flúor (F). Como não há pares isolados no boro, os átomos de flúor se distribuem no mesmo plano, o mais afastados possível uns dos outros.
Outro exemplo é a molécula de eteno (C₂H₄), onde cada átomo de carbono adota uma geometria trigonal plana em relação aos átomos a ele ligados.
É importante notar que se houvesse um par de elétrons isolado no átomo central, a geometria não seria mais trigonal plana, mas sim piramidal, pois o par isolado ocuparia uma das posições do espaço tridimensional.
🔺 Uma forma fácil de lembrar: na geometria trigonal plana, os átomos formam um triângulo perfeito no mesmo plano, sem nenhuma projeção para cima ou para baixo.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A geometria piramidal ocorre quando o átomo central possui três ligantes e um par de elétrons isolados. Esse arranjo forma uma estrutura semelhante a uma pirâmide, com o átomo central no topo e os três ligantes formando a base.
Um exemplo clássico é a molécula de amônia (NH₃), onde o átomo de nitrogênio possui três ligações com hidrogênios e um par de elétrons isolados. O par isolado "empurra" os hidrogênios para baixo, criando a forma piramidal.
Já a geometria tetraédrica aparece quando o átomo central forma quatro ligações (tem quatro pares ligantes) e não possui pares isolados. Os quatro átomos ligantes se posicionam nos vértices de um tetraedro imaginário.
O exemplo mais conhecido é o metano (CH₄), onde o carbono está ligado a quatro átomos de hidrogênio. Os hidrogênios se posicionam o mais distante possível uns dos outros, formando um tetraedro perfeito com ângulos de aproximadamente 109,5° entre as ligações.
💎 Visualize um tetraedro como uma pirâmide de base triangular. Na geometria tetraédrica, o átomo central fica no meio e os quatro ligantes ficam nos vértices.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Para moléculas mais complexas, temos geometrias que acomodam mais ligantes ao redor do átomo central.
A geometria de bipirâmide trigonal acontece quando o átomo central forma cinco ligações (tem cinco pares ligantes). Nesta configuração, três átomos ficam no mesmo plano formando um triângulo equilátero (como na geometria trigonal plana), e os outros dois ficam acima e abaixo desse plano, formando os "polos" da bipirâmide.
Um exemplo desta geometria é o PCl₅ (pentacloreto de fósforo), onde o átomo de fósforo está ligado a cinco átomos de cloro.
A geometria octaédrica ocorre quando o átomo central forma seis ligações (tem seis pares ligantes). Neste caso, os ligantes se posicionam nos vértices de um octaedro, que pode ser visualizado como dois quadrados superpostos e rotacionados 45° um em relação ao outro.
Um exemplo é o SF₆ (hexafluoreto de enxofre), onde o enxofre está ligado a seis átomos de flúor em uma disposição octaédrica.
🧩 Estas geometrias moleculares mais complexas são importantes em compostos usados em medicamentos, catalisadores e materiais avançados.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Os ângulos entre as ligações são uma consequência direta da geometria molecular. Eles expressam numericamente como os átomos estão organizados no espaço tridimensional.
Cada geometria tem seus ângulos característicos:
Esses ângulos ocorrem porque os átomos e os pares de elétrons tendem a se posicionar o mais distante possível uns dos outros. Esta é a base da Teoria da Repulsão dos Pares de Elétrons da Camada de Valência (VSEPR), que explica a geometria das moléculas.
Os pares isolados (não ligantes) exercem uma repulsão maior que os pares ligantes, o que pode alterar ligeiramente os ângulos ideais. Por exemplo, na água (H₂O), o ângulo é aproximadamente 104,5° em vez dos 109,5° de uma tetraédrica perfeita.
🧭 Os ângulos de ligação são como uma bússola para entender a estrutura molecular. Eles nos ajudam a prever como a molécula interage com outras substâncias.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
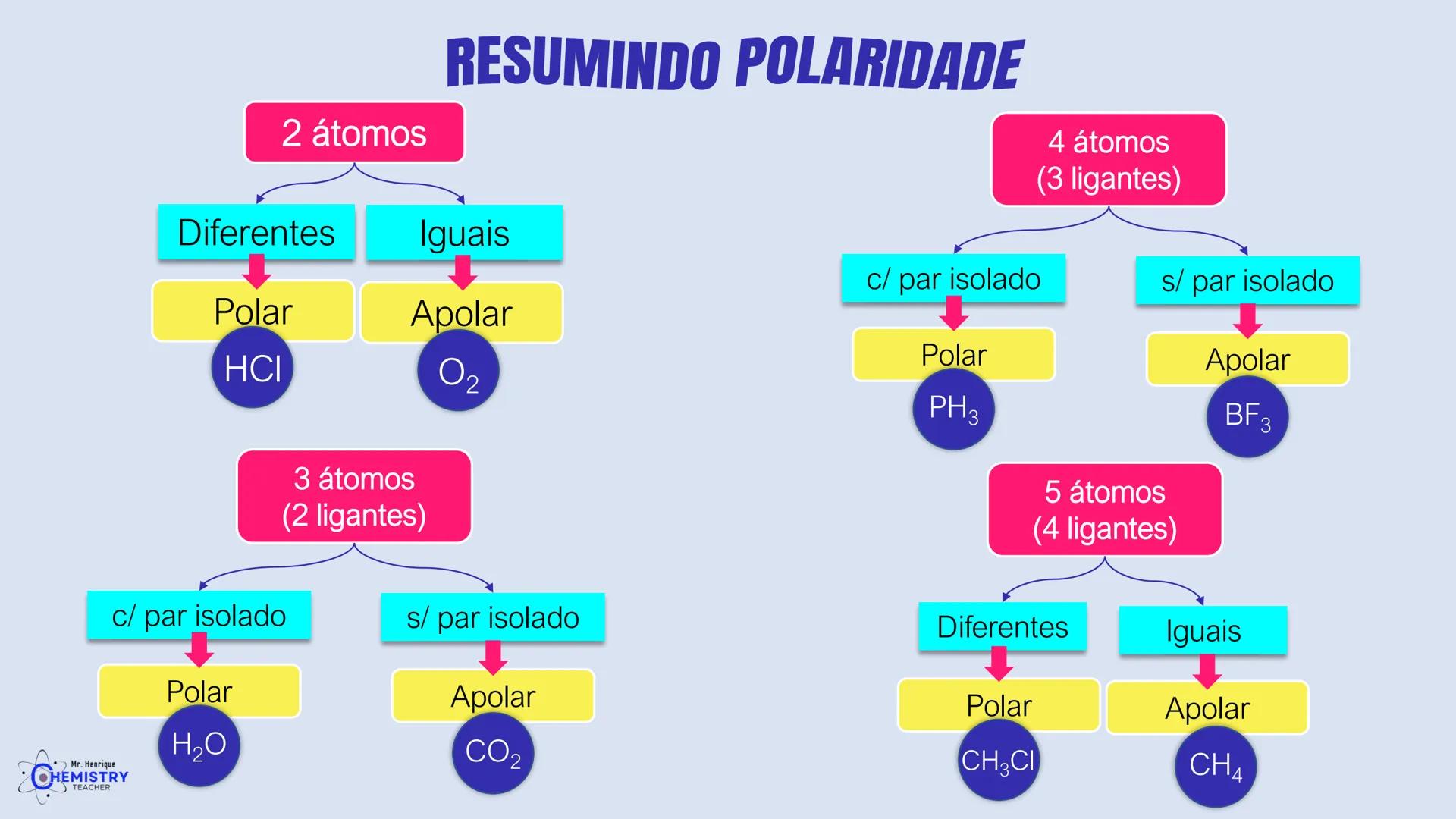
Vamos organizar o que aprendemos sobre geometria molecular de forma prática:
Para moléculas com 2 átomos:
Para moléculas com 3 átomos (2 ligantes no átomo central):
Para moléculas com 4 átomos (3 ligantes no átomo central):
Para moléculas com 5 átomos (4 ligantes no átomo central):
A chave para determinar a geometria molecular é contar tanto os átomos ligantes quanto os pares de elétrons isolados ao redor do átomo central, e entender como eles se repelem entre si.
📏 Uma dica para facilitar: conte primeiro o número total de pares de elétrons ao redor do átomo central para determinar a "geometria eletrônica", depois veja quantos desses pares são realmente ligantes para determinar a geometria molecular.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
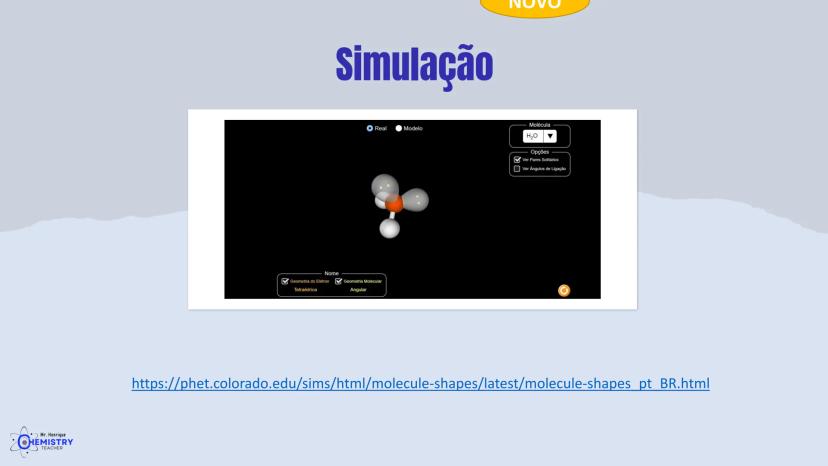
As simulações computacionais são ferramentas poderosas para visualizar e compreender a geometria molecular. Elas permitem que você veja as moléculas em três dimensões e entenda como os átomos estão arranjados no espaço.
A simulação PhET do Colorado é um recurso excelente que permite:
Estas ferramentas interativas ajudam a compreender como a repulsão entre os pares de elétrons determina a forma das moléculas. Você pode, por exemplo, adicionar ou remover ligantes e pares isolados para ver como a geometria se altera.
Ao explorar moléculas como a água (H₂O) na simulação, você pode observar sua geometria angular e entender por que esse arranjo é crucial para as propriedades únicas da água.
💻 Experimente a simulação! É uma maneira divertida e interativa de aprender sobre geometria molecular - muito melhor que apenas ler sobre isso no livro.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Nosso companheiro de IA foi criado especificamente para atender às necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos oferecer respostas realmente relevantes e significativas. Mas não se trata apenas de respostas, o companheiro também está aqui para guiar você pelos desafios diários de aprendizado, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização com base nas suas habilidades e desenvolvimentos.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
36
Ferramentas Inteligentes NOVO
Transforme esta anotação em: ✓ 50+ Questões de Prática ✓ Flashcards Interativos ✓ Simulado Completo ✓ Esquemas de Redação
App Store
Google Play
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS