Vamos estudar as Funções Inorgânicas! Esse tema explica como substâncias... Mostrar mais
Cadastre-se para ver o conteúdoÉ grátis!
Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Knowunity AI
Matérias
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos os tópicos
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos os tópicos
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos os tópicos
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos os tópicos
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos os tópicos
222
•
Atualizado May 4, 2026
•
Isabella Oliveira
@isabellao_q7dsb
Vamos estudar as Funções Inorgânicas! Esse tema explica como substâncias... Mostrar mais




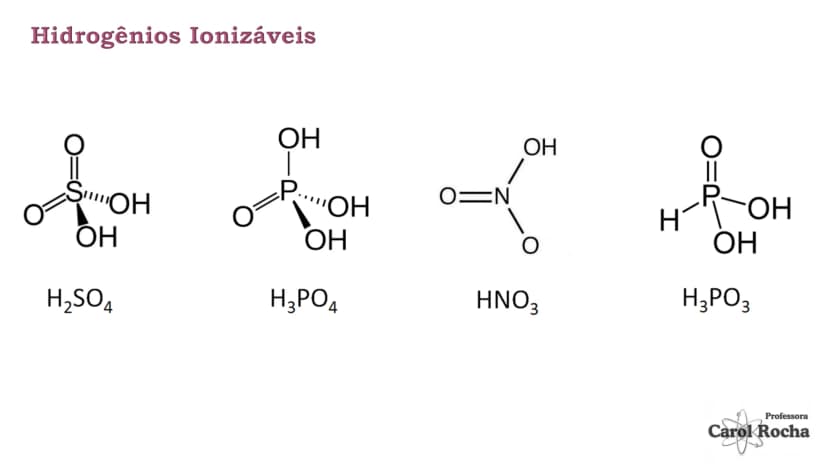


As funções inorgânicas são substâncias químicas que geralmente não possuem carbono ou, quando possuem, não apresentam ligações carbono-hidrogênio. Os principais grupos são: ácidos (H2SO4, HNO3), bases (NaOH, Mg(OH)2), sais (NaNO3, K3PO4) e óxidos (SO3, CuO).
Essas substâncias estão por toda parte! O ácido cítrico da laranja, o hidróxido de magnésio do leite de magnésia, o cloreto de sódio (sal de cozinha) e o dióxido de carbono que respiramos são exemplos de compostos inorgânicos.
Cada grupo tem características próprias que determinam como reagem entre si e com outros compostos, sendo fundamentais para entender processos industriais, biológicos e ambientais.
💡 Lembre-se: Nem todo composto com carbono é orgânico! CO2 e CaCO3 (calcário) são inorgânicos porque não apresentam ligações C-H.

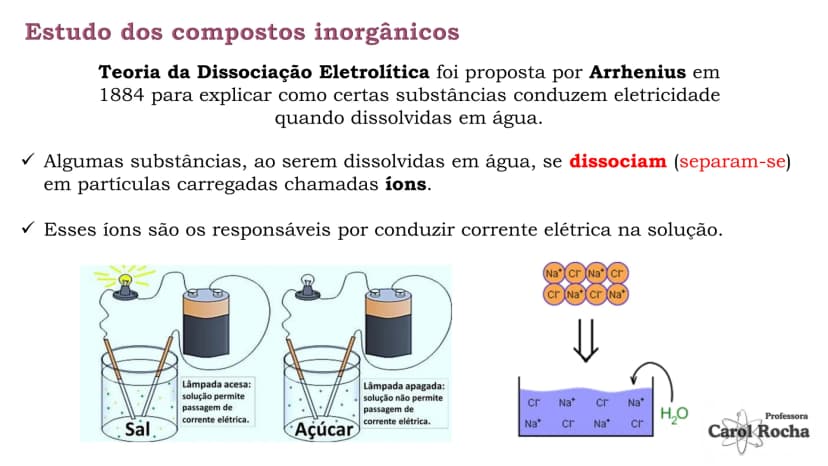
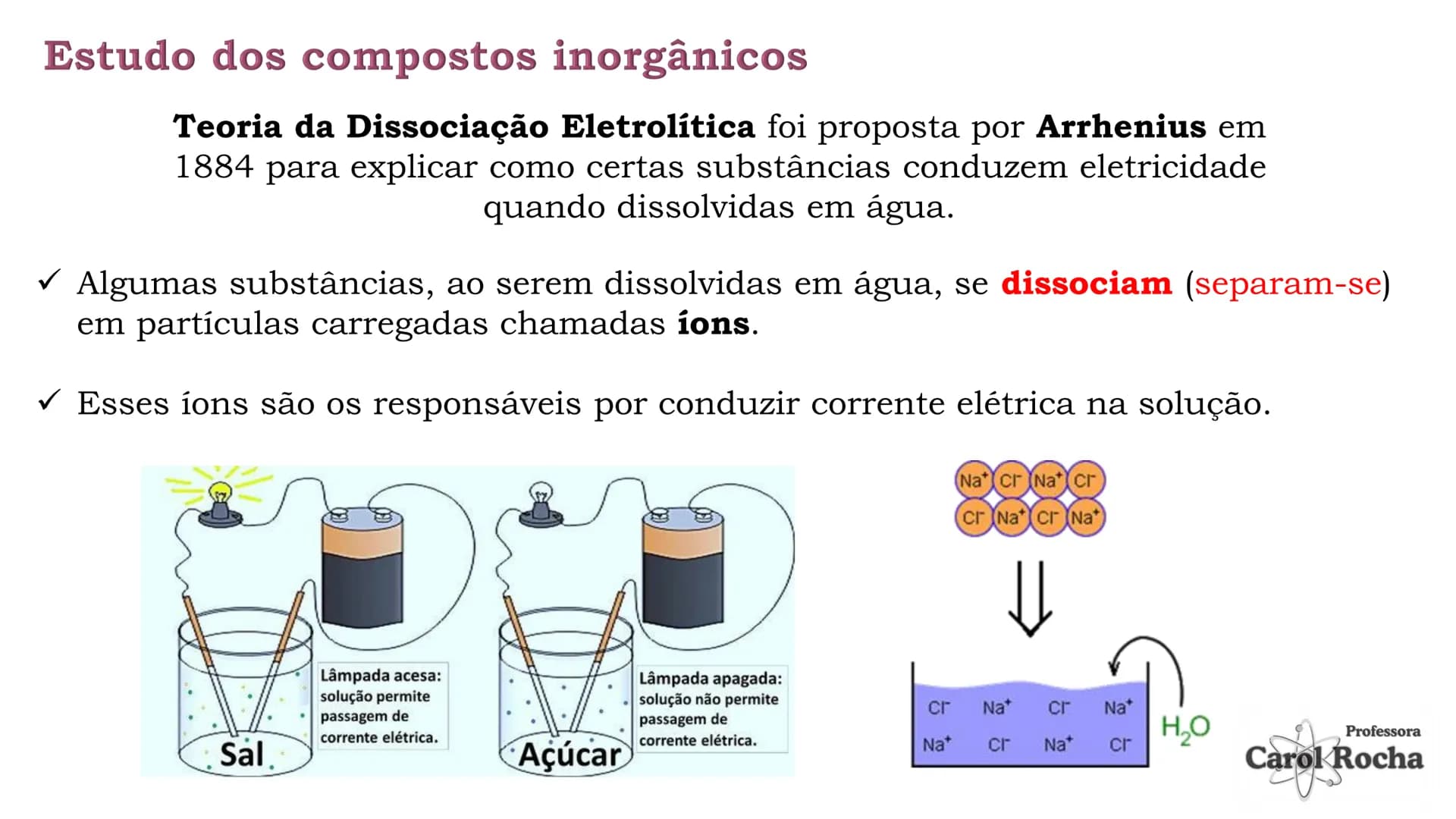
A Teoria da Dissociação Eletrolítica, proposta por Arrhenius em 1884, explica como certas substâncias conseguem conduzir eletricidade quando dissolvidas em água. É uma teoria revolucionária que mudou nossa compreensão da química!
Quando substâncias como o sal de cozinha (NaCl) são dissolvidas em água, elas se separam em partículas carregadas chamadas íons . Esses íons livres são responsáveis por conduzir corrente elétrica na solução.
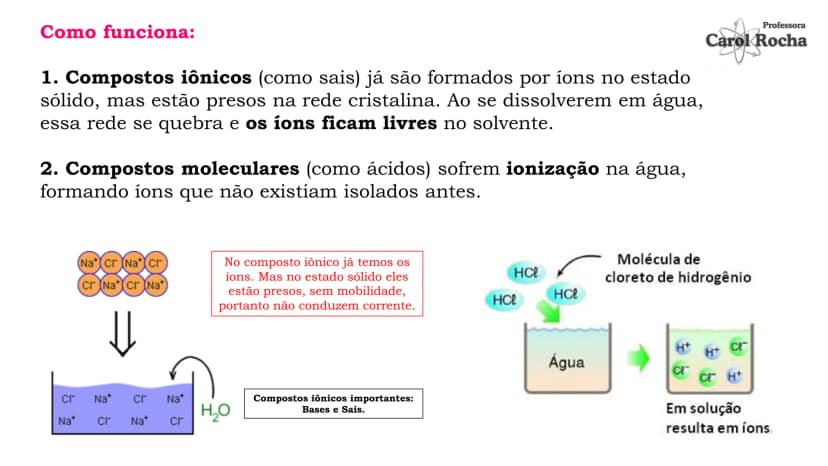
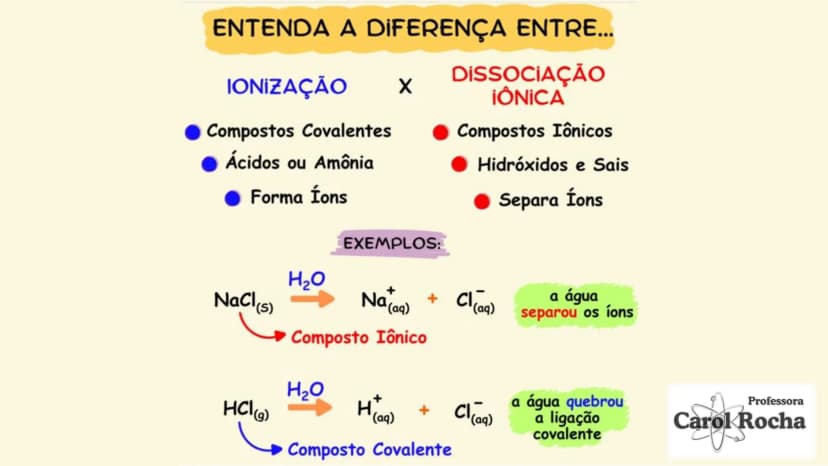
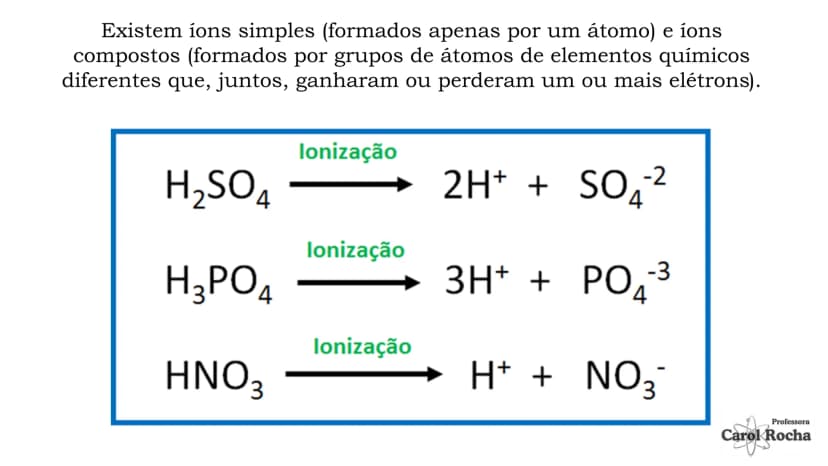
Existem dois processos importantes: a dissociação iônica (separação de íons que já existiam no composto sólido) e a ionização (formação de íons a partir de moléculas neutras). Os compostos iônicos como sais e bases sofrem dissociação, enquanto compostos moleculares como ácidos sofrem ionização.
🔍 Entenda a diferença: Na dissociação, os íons já existem no composto (como no NaCl); na ionização, os íons são formados na água (como no HCl).
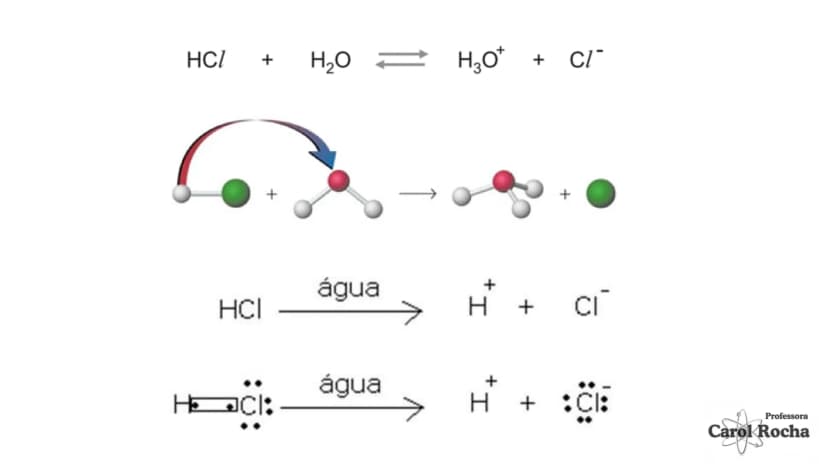
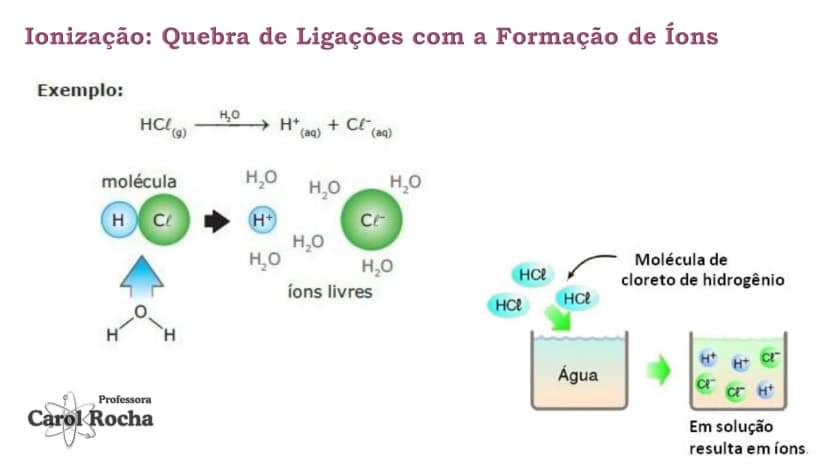
Segundo a teoria de Arrhenius, ácidos são substâncias moleculares que, em solução aquosa, sofrem ionização, liberando como cátion o H⁺. É um processo em que ligações covalentes são rompidas, formando íons.
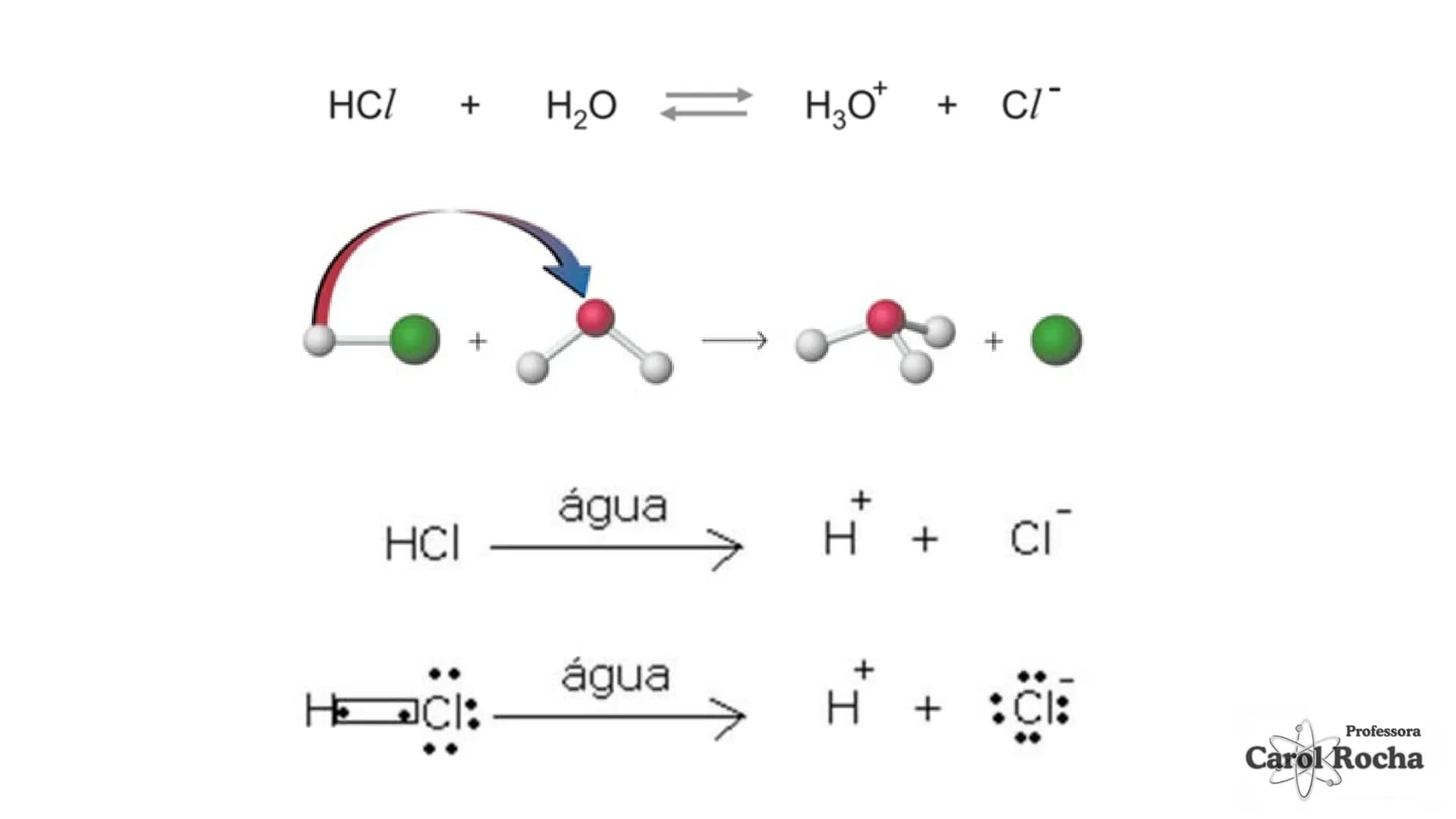
Na realidade, o íon H⁺ não existe livre em solução - ele se une rapidamente a uma molécula de água, formando o íon hidroxônio (H₃O⁺). Por isso, quando um ácido como HCl se dissolve em água, ocorre: HCl + H₂O → H₃O⁺ + Cl⁻.
Os ácidos são classificados quanto à sua força: ácidos fortes (α > 50%, como HCl, H₂SO₄) se ionizam quase completamente; ácidos moderados (5% ≤ α ≤ 50%, como H₃PO₄) se ionizam parcialmente; e ácidos fracos (α < 5%, como HCN) se ionizam pouco.
🧪 Curiosidade: A força de um ácido é medida pelo seu grau de ionização (α), que é a porcentagem de moléculas que se ionizam em solução aquosa.
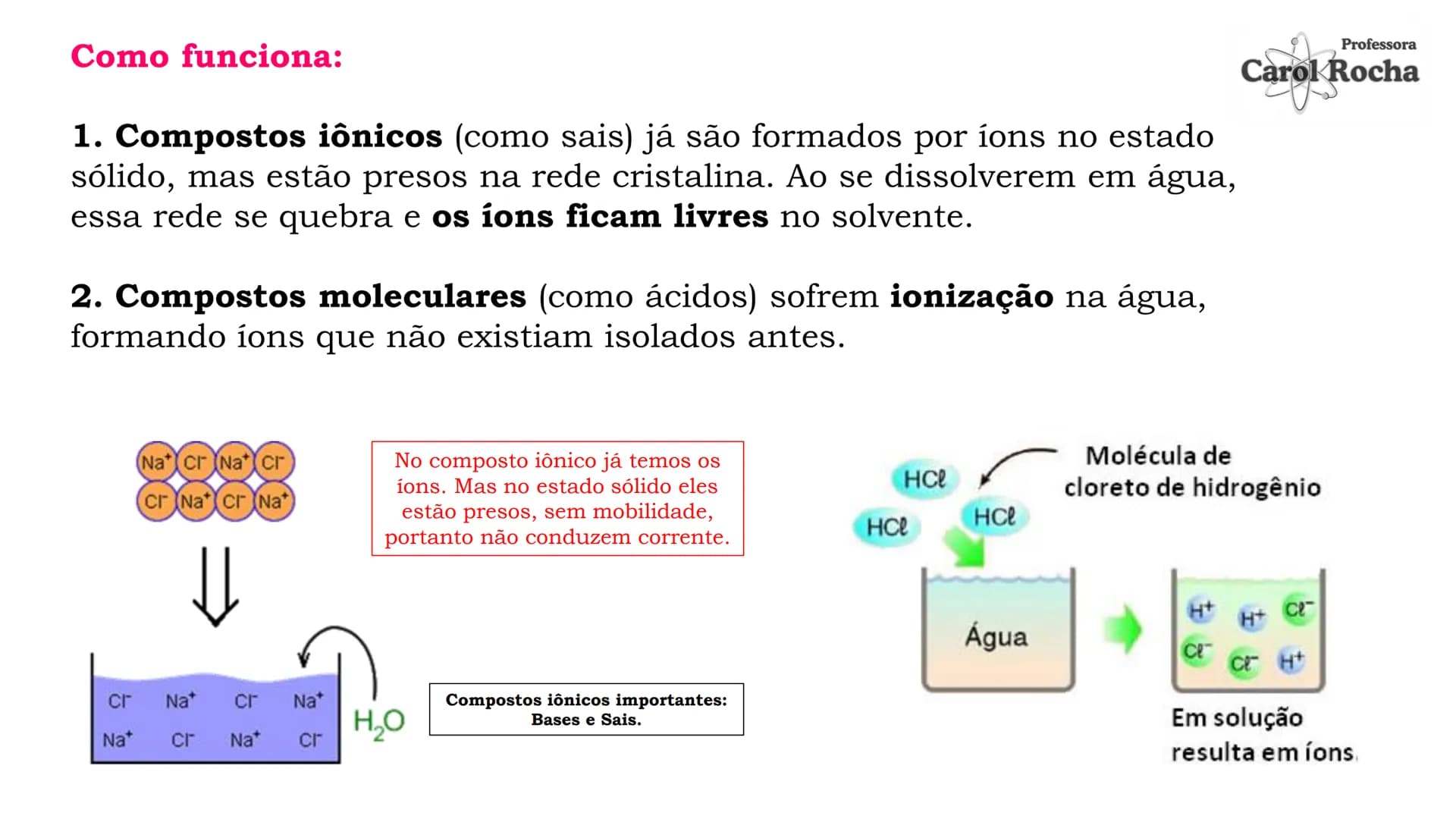
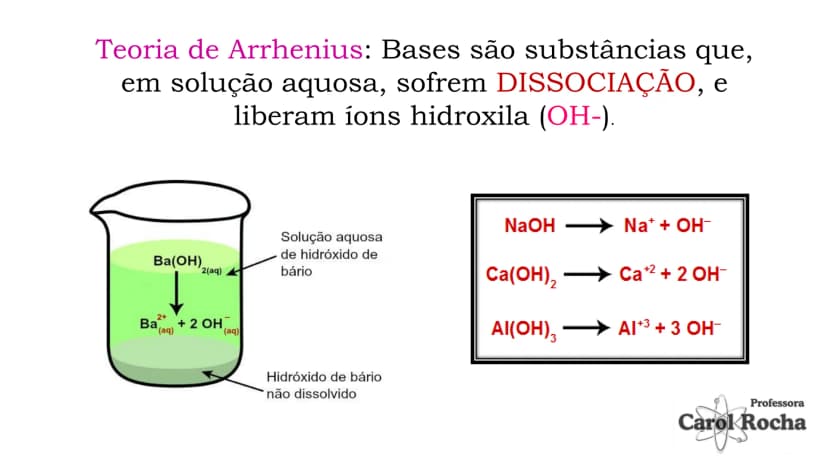
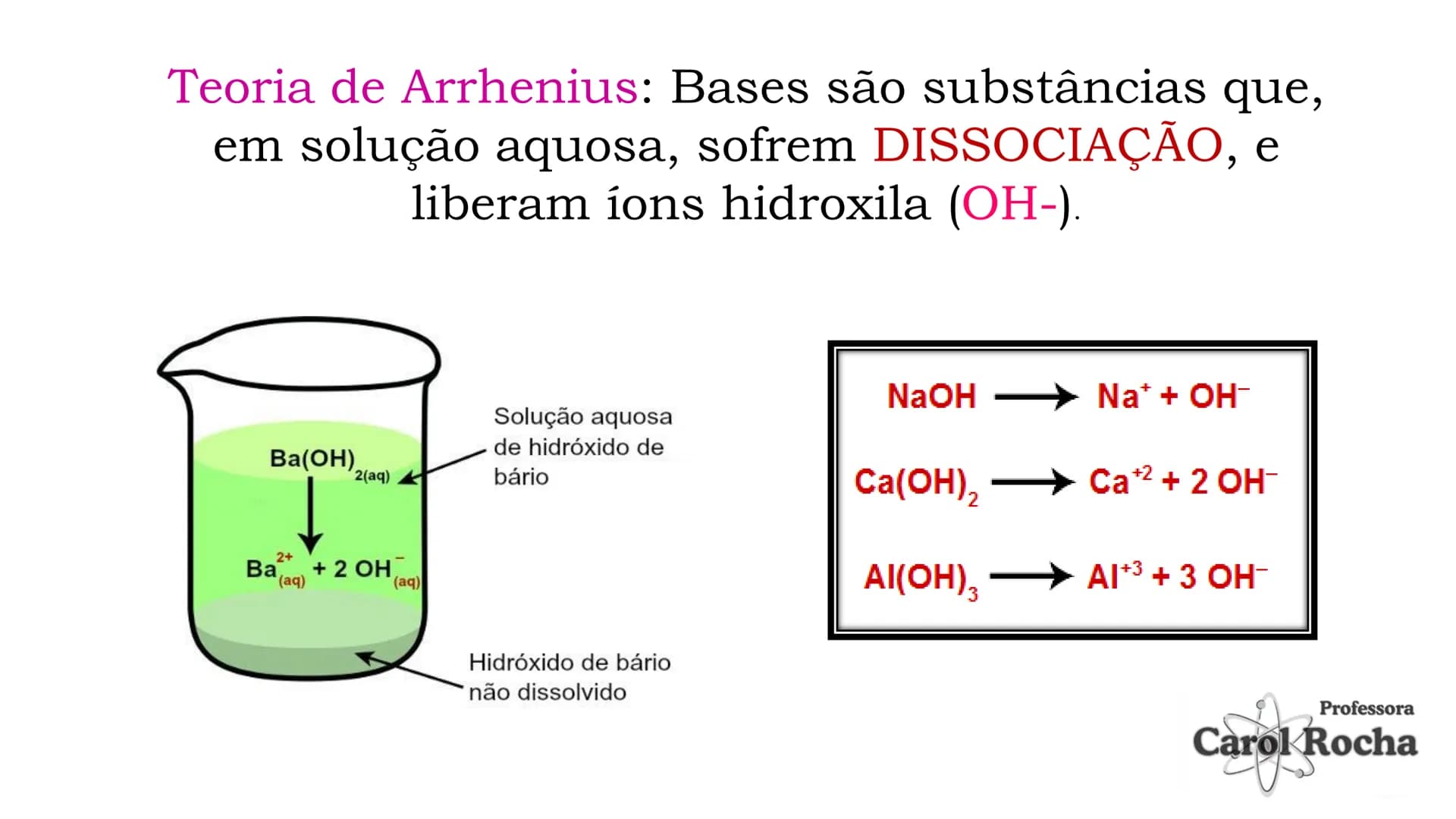
Bases, segundo Arrhenius, são substâncias que em solução aquosa sofrem dissociação e liberam íons hidroxila . A dissociação é um processo físico onde os íons que já existiam no composto sólido se separam na água.
Quando hidróxido de sódio (NaOH) se dissolve em água, ele se dissocia: NaOH → Na⁺ + OH⁻. O mesmo acontece com bases como Ca(OH)₂ → Ca²⁺ + 2OH⁻ e Al(OH)₃ → Al³⁺ + 3OH⁻.
Assim como os ácidos, as bases também são classificadas pela sua força. Bases fortes (α ≈ 100%, como NaOH e KOH) se dissociam completamente, enquanto bases fracas (α < 5%, como NH₄OH) se dissociam pouco em solução aquosa.
💦 Dica prática: Para identificar uma base, observe se ela possui o grupo OH ligado a um metal. Exemplos: NaOH, Mg(OH)₂, Al(OH)₃.
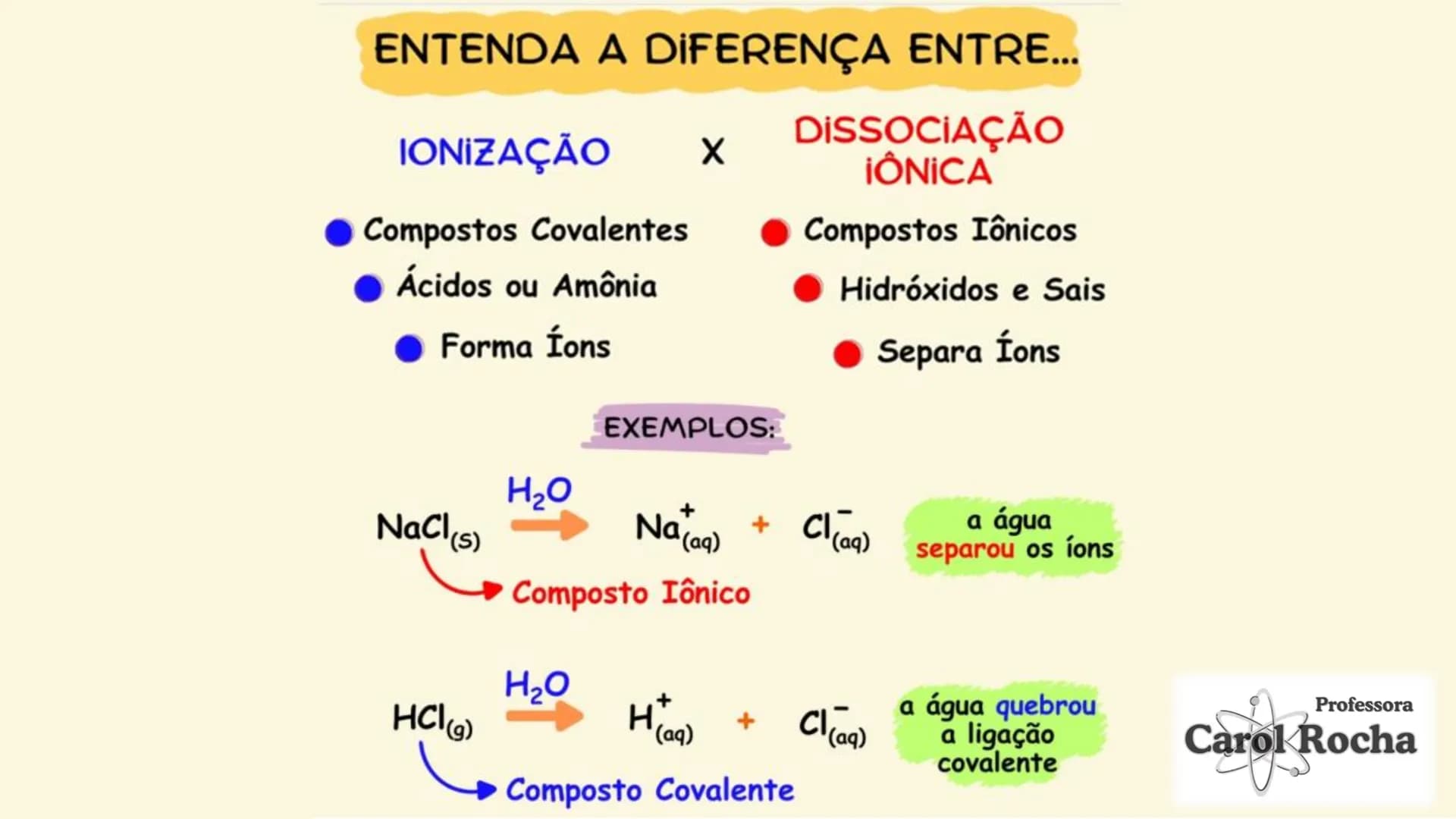
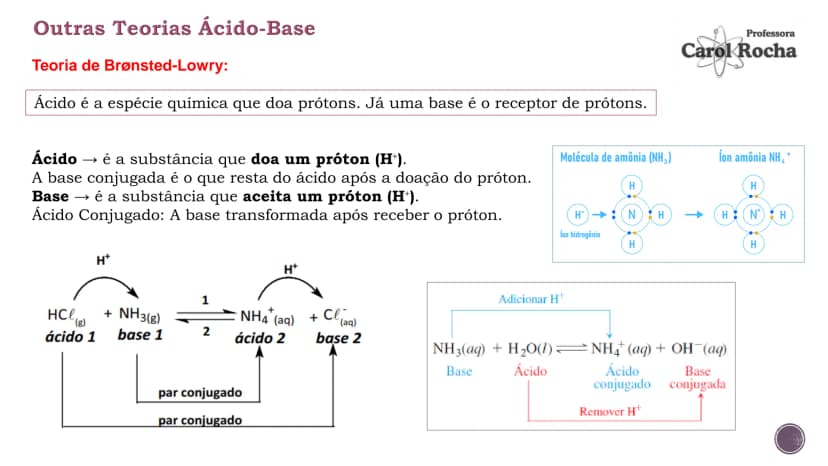
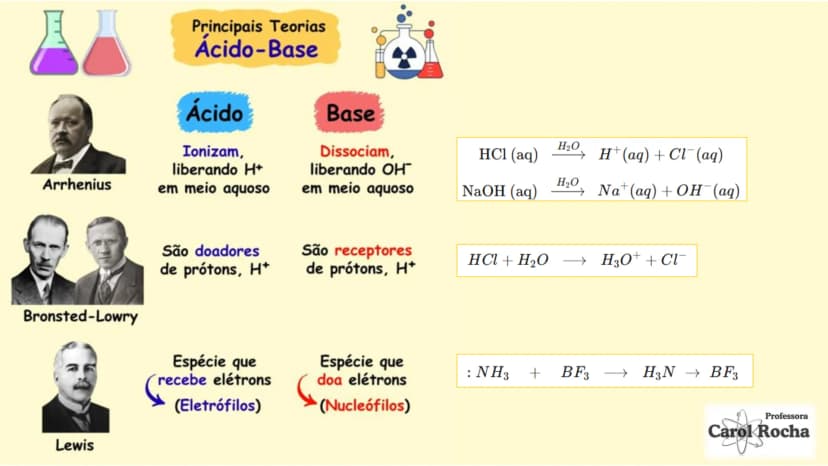
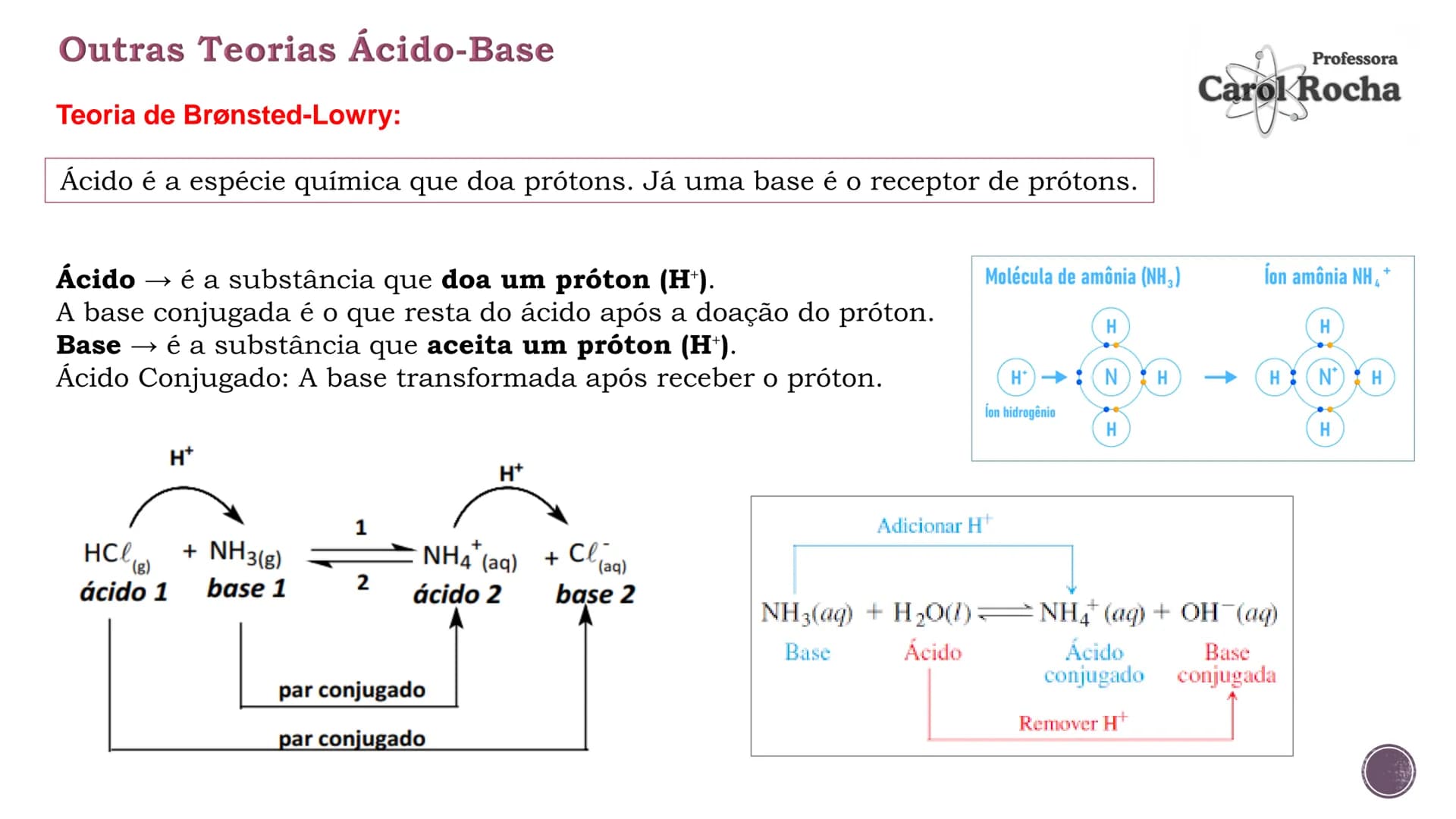
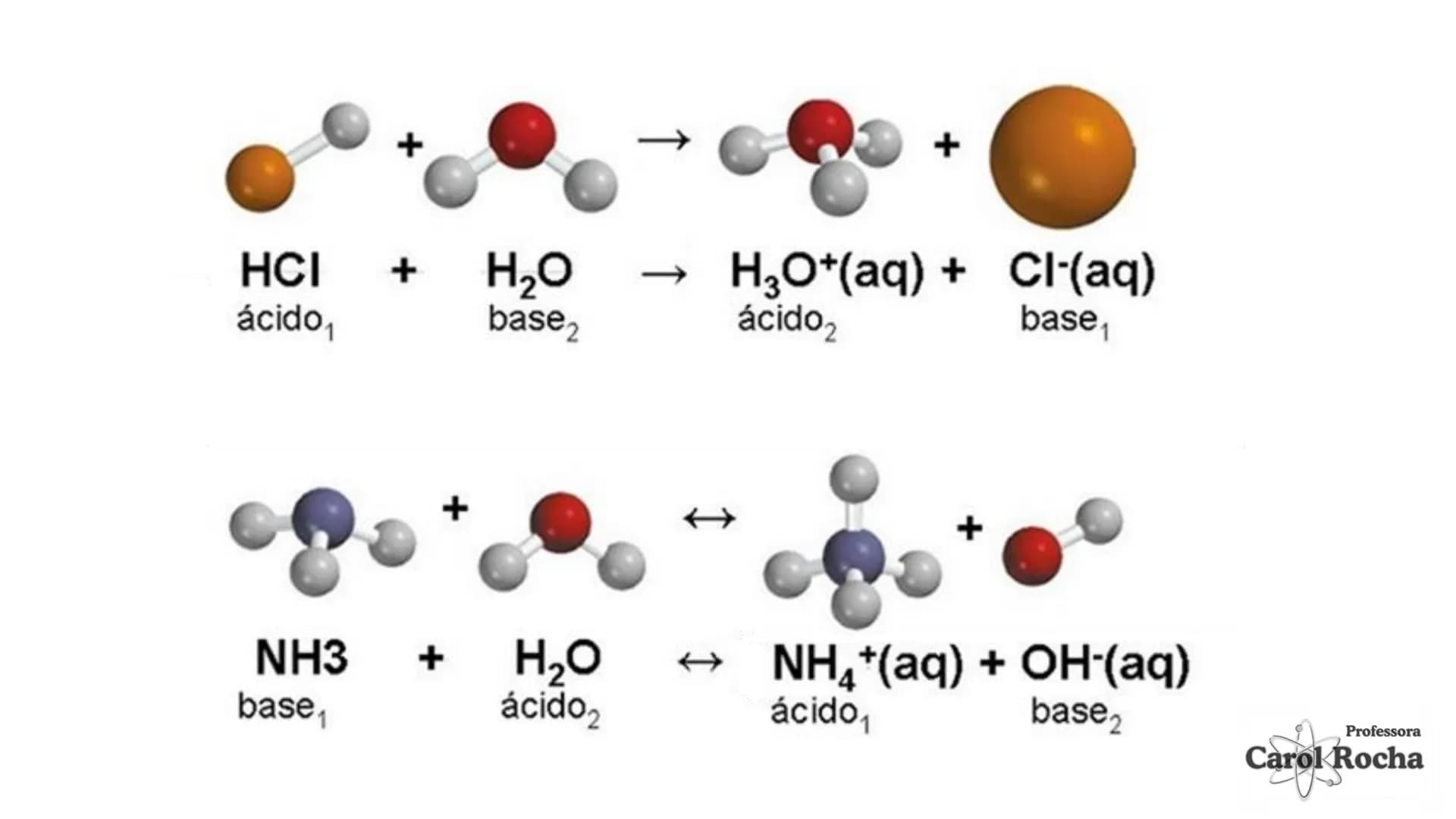
A teoria de Brønsted-Lowry amplia nossa compreensão sobre ácidos e bases. Nela, um ácido é qualquer substância que doa prótons (H⁺), e uma base é a que aceita prótons. Por exemplo: HCl + NH₃ → NH₄⁺ + Cl⁻ (HCl doa H⁺, NH₃ aceita H⁺).
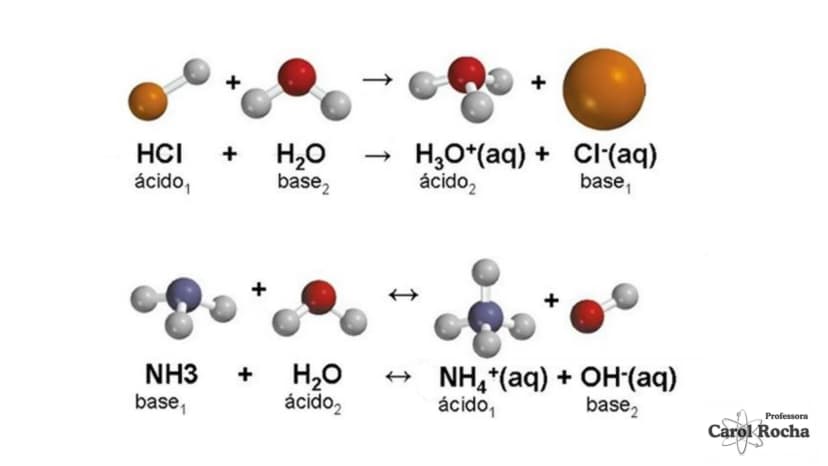
Esta teoria introduz o conceito de pares conjugados: quando um ácido doa um próton, resta sua base conjugada; quando uma base aceita um próton, forma-se seu ácido conjugado. Na reação HCl + H₂O → H₃O⁺ + Cl⁻, o Cl⁻ é a base conjugada de HCl, e H₃O⁺ é o ácido conjugado de H₂O.
Já a teoria de Lewis vai além, definindo ácidos como receptores de pares de elétrons e bases como doadoras de pares de elétrons. Esta definição abrange reações sem transferência de H⁺, como quando NH₃ (doa par de elétrons) reage com BF₃ (aceita par de elétrons).
🔬 Amplie seu conhecimento: A teoria de Lewis é a mais abrangente e explica reações ácido-base que as outras teorias não conseguem explicar!

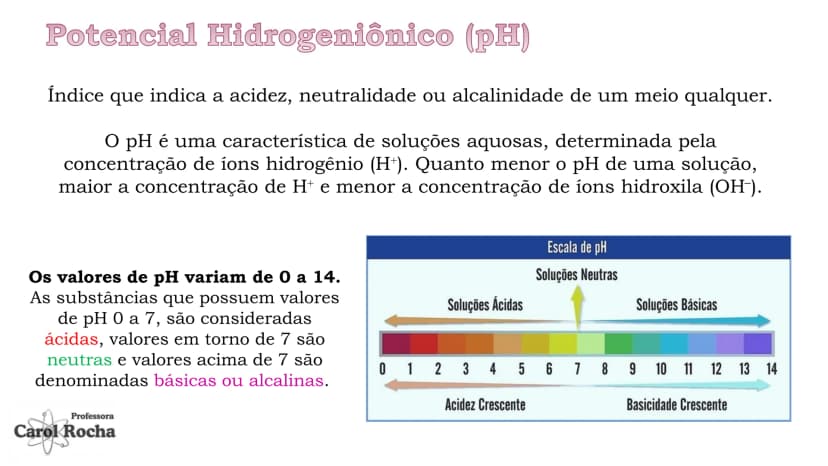
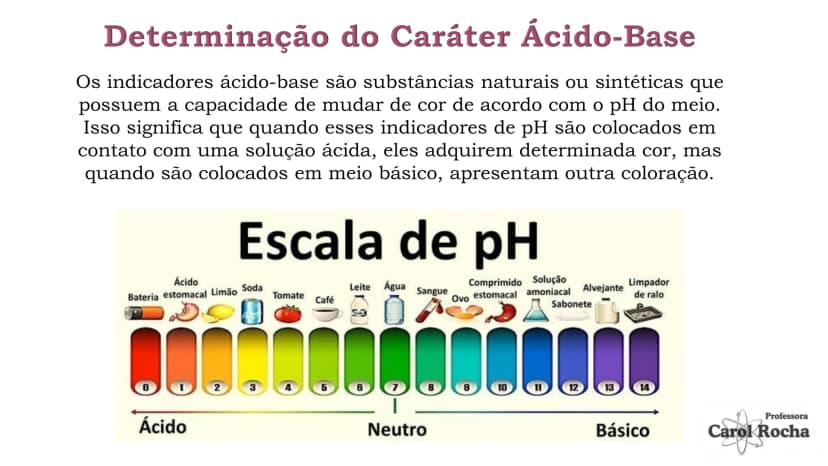
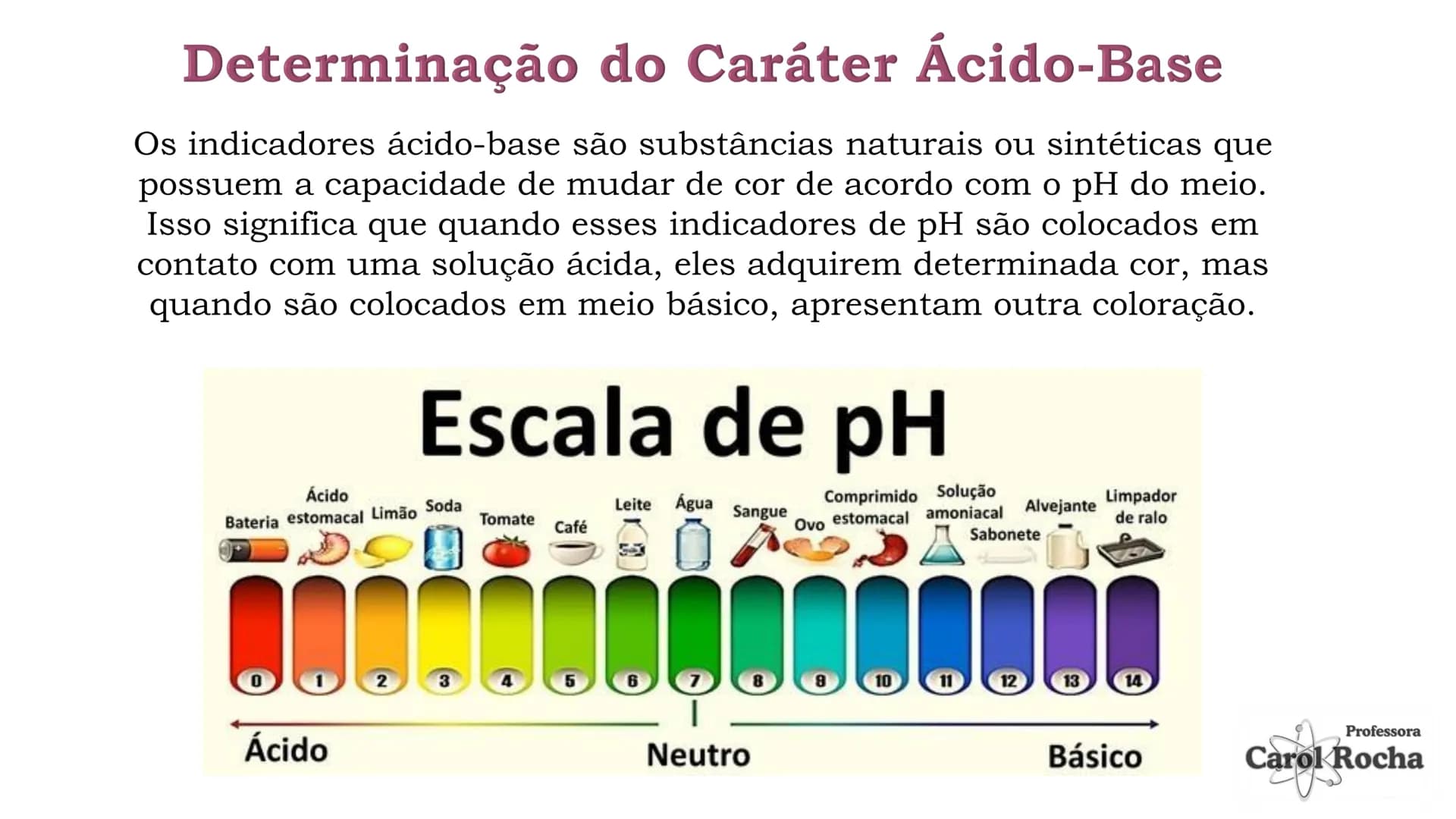
O potencial hidrogeniônico (pH) é uma escala que mede a acidez ou basicidade de uma solução. Variando de 0 a 14, o pH indica a concentração de íons H⁺ na solução: quanto menor o pH, mais ácida é a solução; quanto maior, mais básica.
Soluções com pH menor que 7 são ácidas (como limão, pH≈2), pH igual a 7 são neutras (água pura), e pH maior que 7 são básicas . Esta escala é logarítmica, então cada unidade representa uma mudança de 10 vezes na concentração de H⁺!
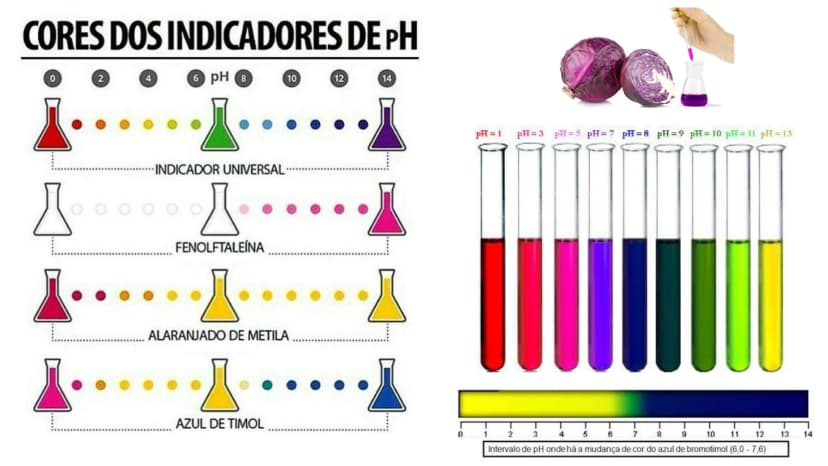
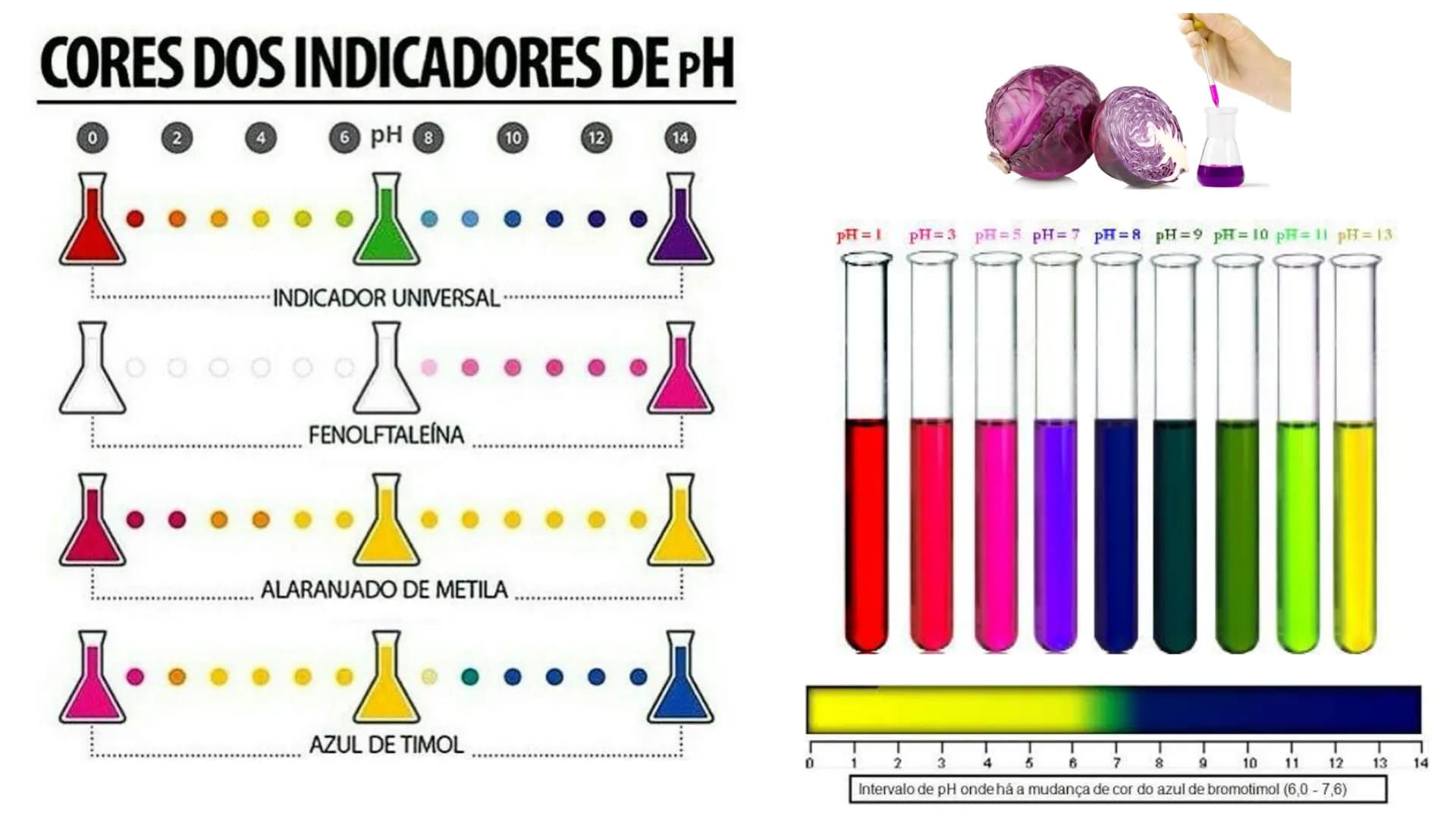
Para identificar o pH, usamos indicadores ácido-base, substâncias que mudam de cor conforme o pH do meio. A fenolftaleína fica incolor em meio ácido e rosa em meio básico, enquanto o papel tornassol azul fica vermelho em meio ácido e mantém a cor azul em meio básico.
🌈 Experimento caseiro: Use suco de repolho roxo como indicador natural! Ele fica vermelho em meios muito ácidos, roxo em meios neutros e verde/amarelo em meios básicos.
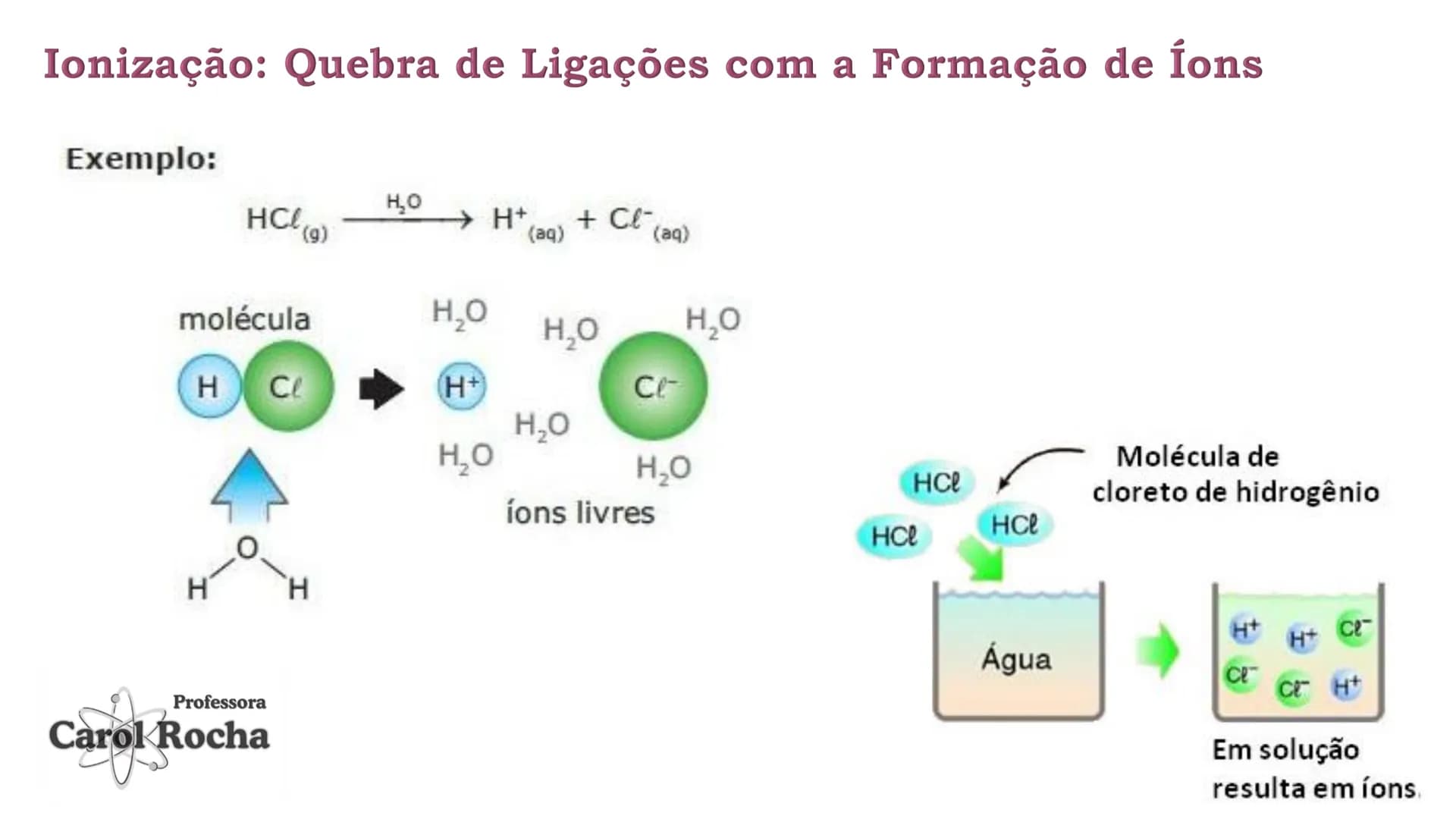


Nosso companheiro de IA foi criado especificamente para atender às necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos oferecer respostas realmente relevantes e significativas. Mas não se trata apenas de respostas, o companheiro também está aqui para guiar você pelos desafios diários de aprendizado, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização com base nas suas habilidades e desenvolvimentos.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
App Store
Google Play
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
Isabella Oliveira
@isabellao_q7dsb
Vamos estudar as Funções Inorgânicas! Esse tema explica como substâncias que não contêm ligações carbono-hidrogênio se comportam quimicamente. Entender ácidos, bases, sais e óxidos é essencial para compreender reações químicas do nosso cotidiano.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
As funções inorgânicas são substâncias químicas que geralmente não possuem carbono ou, quando possuem, não apresentam ligações carbono-hidrogênio. Os principais grupos são: ácidos (H2SO4, HNO3), bases (NaOH, Mg(OH)2), sais (NaNO3, K3PO4) e óxidos (SO3, CuO).
Essas substâncias estão por toda parte! O ácido cítrico da laranja, o hidróxido de magnésio do leite de magnésia, o cloreto de sódio (sal de cozinha) e o dióxido de carbono que respiramos são exemplos de compostos inorgânicos.
Cada grupo tem características próprias que determinam como reagem entre si e com outros compostos, sendo fundamentais para entender processos industriais, biológicos e ambientais.
💡 Lembre-se: Nem todo composto com carbono é orgânico! CO2 e CaCO3 (calcário) são inorgânicos porque não apresentam ligações C-H.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
A Teoria da Dissociação Eletrolítica, proposta por Arrhenius em 1884, explica como certas substâncias conseguem conduzir eletricidade quando dissolvidas em água. É uma teoria revolucionária que mudou nossa compreensão da química!
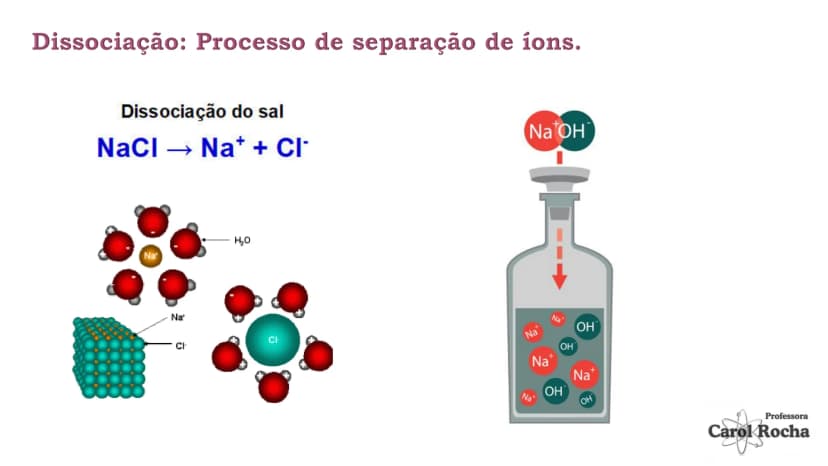
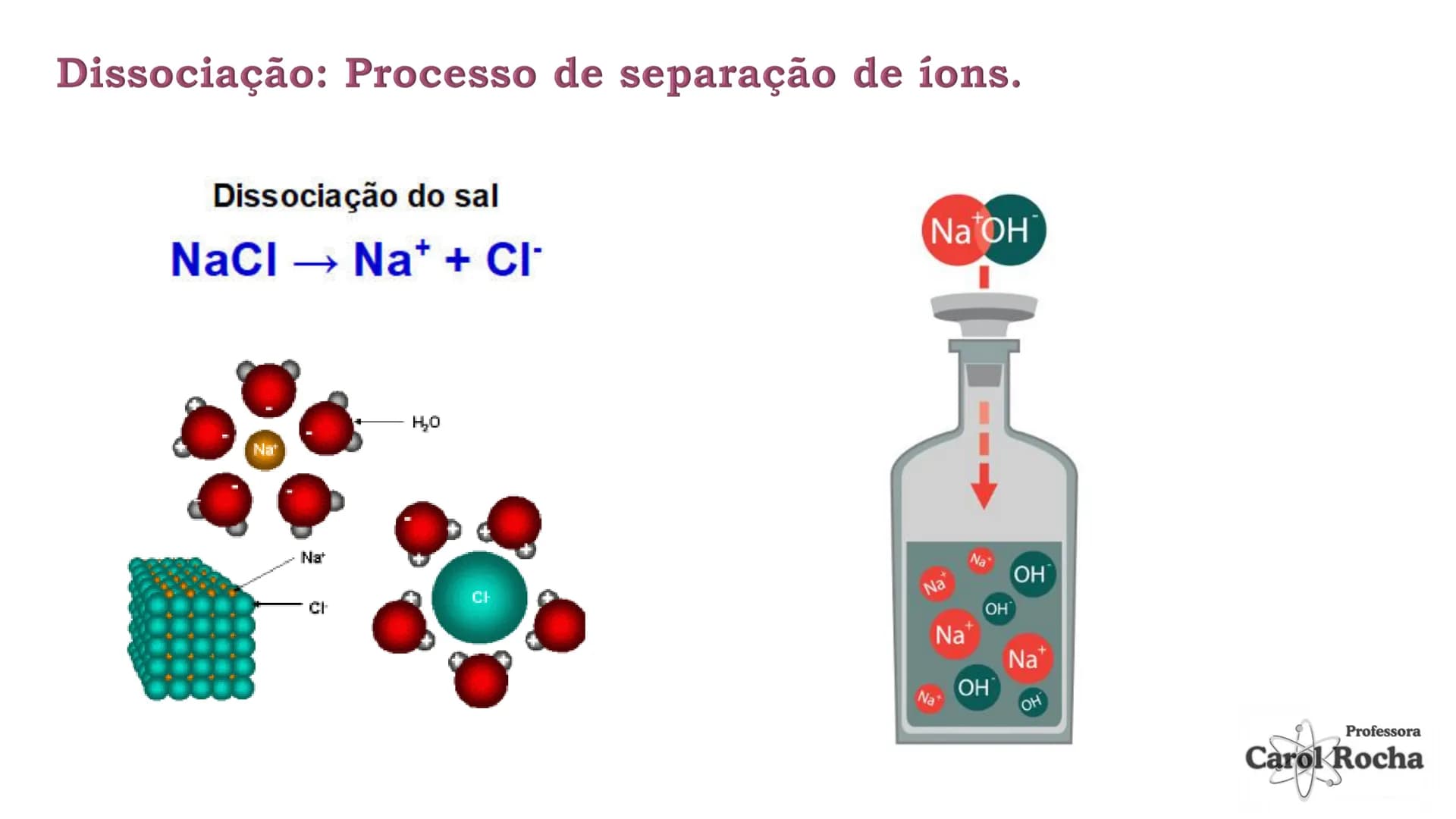
Quando substâncias como o sal de cozinha (NaCl) são dissolvidas em água, elas se separam em partículas carregadas chamadas íons . Esses íons livres são responsáveis por conduzir corrente elétrica na solução.
Existem dois processos importantes: a dissociação iônica (separação de íons que já existiam no composto sólido) e a ionização (formação de íons a partir de moléculas neutras). Os compostos iônicos como sais e bases sofrem dissociação, enquanto compostos moleculares como ácidos sofrem ionização.
🔍 Entenda a diferença: Na dissociação, os íons já existem no composto (como no NaCl); na ionização, os íons são formados na água (como no HCl).

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
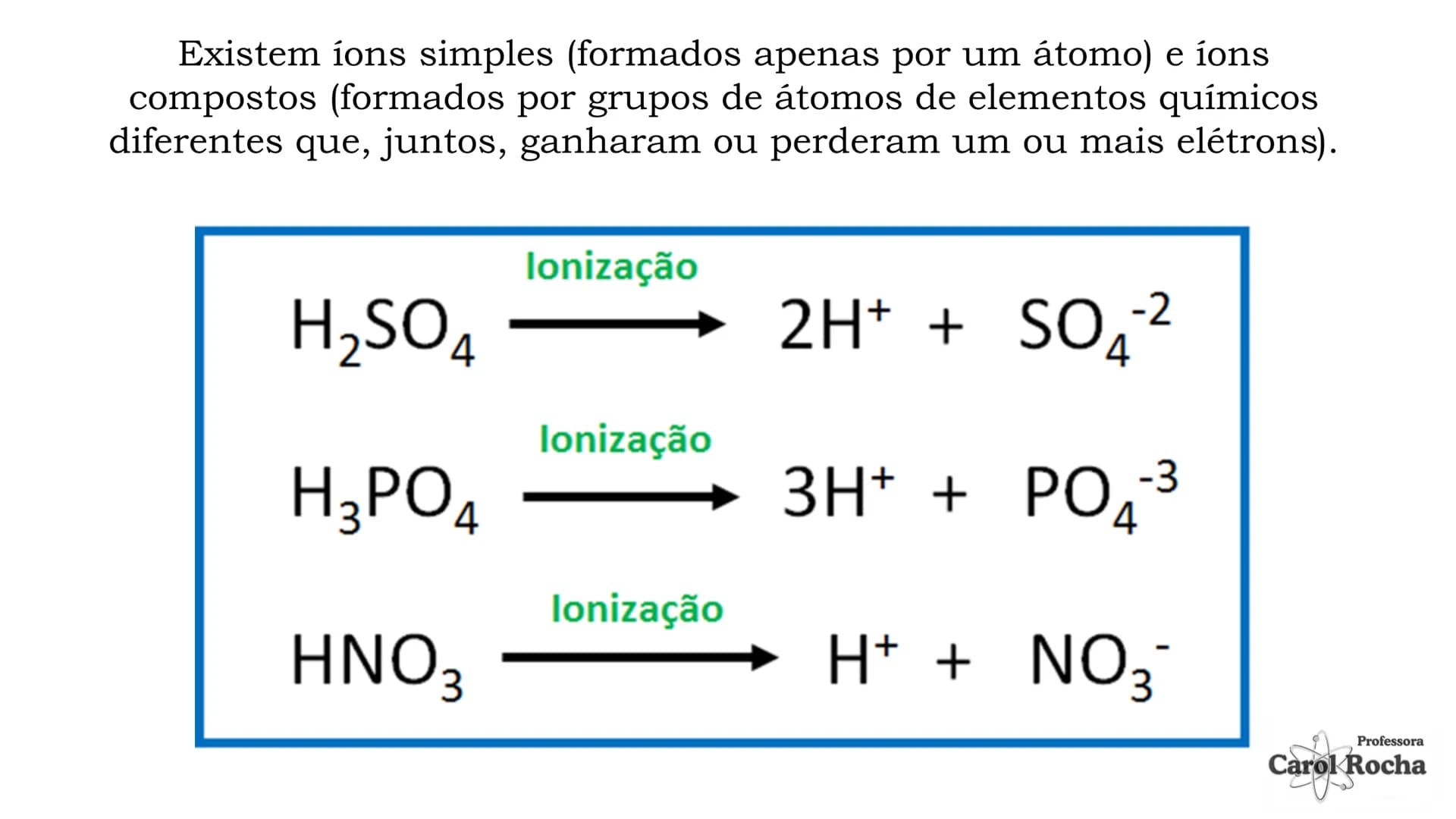
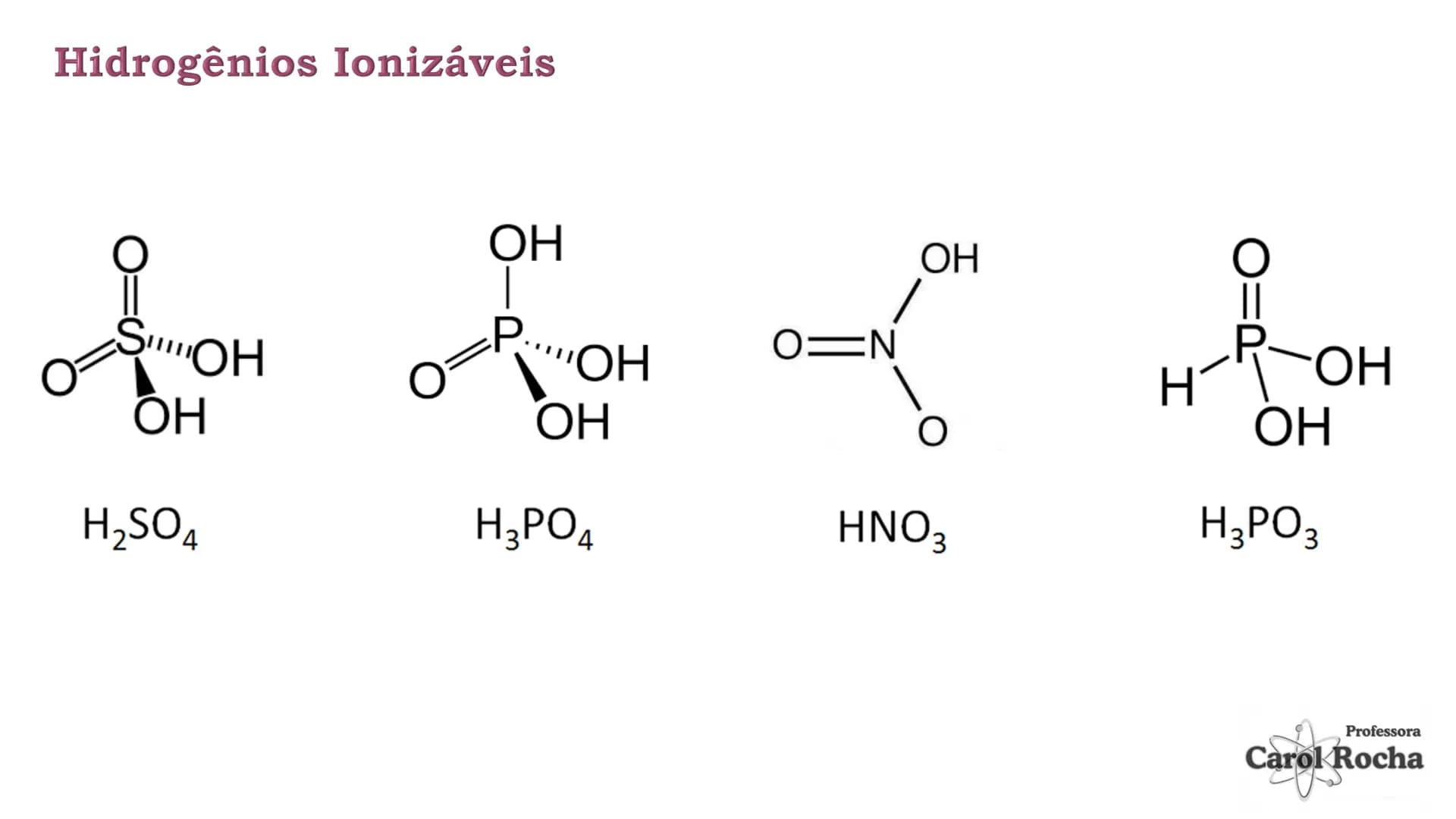
Segundo a teoria de Arrhenius, ácidos são substâncias moleculares que, em solução aquosa, sofrem ionização, liberando como cátion o H⁺. É um processo em que ligações covalentes são rompidas, formando íons.
Na realidade, o íon H⁺ não existe livre em solução - ele se une rapidamente a uma molécula de água, formando o íon hidroxônio (H₃O⁺). Por isso, quando um ácido como HCl se dissolve em água, ocorre: HCl + H₂O → H₃O⁺ + Cl⁻.
Os ácidos são classificados quanto à sua força: ácidos fortes (α > 50%, como HCl, H₂SO₄) se ionizam quase completamente; ácidos moderados (5% ≤ α ≤ 50%, como H₃PO₄) se ionizam parcialmente; e ácidos fracos (α < 5%, como HCN) se ionizam pouco.
🧪 Curiosidade: A força de um ácido é medida pelo seu grau de ionização (α), que é a porcentagem de moléculas que se ionizam em solução aquosa.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Bases, segundo Arrhenius, são substâncias que em solução aquosa sofrem dissociação e liberam íons hidroxila . A dissociação é um processo físico onde os íons que já existiam no composto sólido se separam na água.
Quando hidróxido de sódio (NaOH) se dissolve em água, ele se dissocia: NaOH → Na⁺ + OH⁻. O mesmo acontece com bases como Ca(OH)₂ → Ca²⁺ + 2OH⁻ e Al(OH)₃ → Al³⁺ + 3OH⁻.
Assim como os ácidos, as bases também são classificadas pela sua força. Bases fortes (α ≈ 100%, como NaOH e KOH) se dissociam completamente, enquanto bases fracas (α < 5%, como NH₄OH) se dissociam pouco em solução aquosa.
💦 Dica prática: Para identificar uma base, observe se ela possui o grupo OH ligado a um metal. Exemplos: NaOH, Mg(OH)₂, Al(OH)₃.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
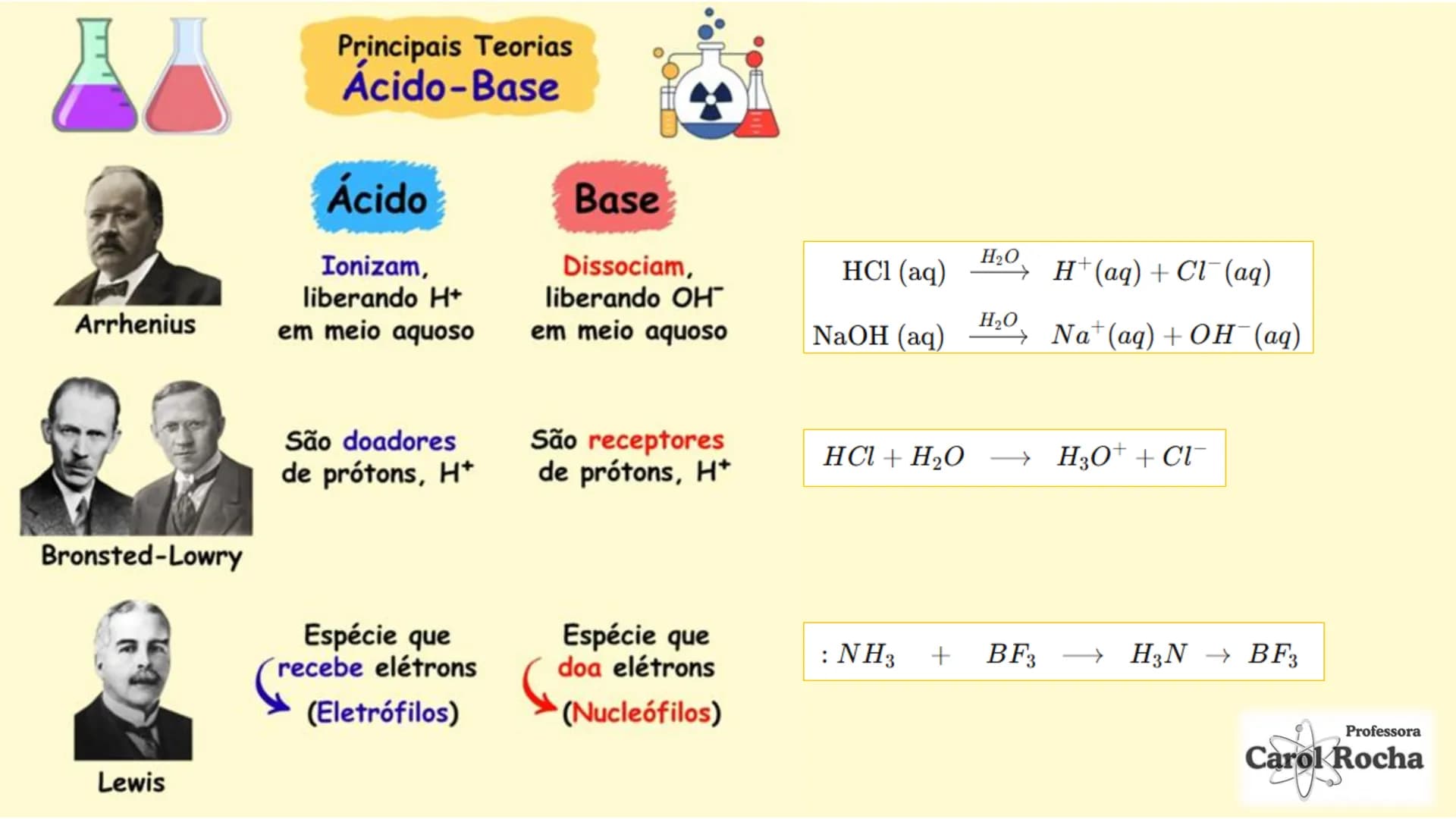
A teoria de Brønsted-Lowry amplia nossa compreensão sobre ácidos e bases. Nela, um ácido é qualquer substância que doa prótons (H⁺), e uma base é a que aceita prótons. Por exemplo: HCl + NH₃ → NH₄⁺ + Cl⁻ (HCl doa H⁺, NH₃ aceita H⁺).
Esta teoria introduz o conceito de pares conjugados: quando um ácido doa um próton, resta sua base conjugada; quando uma base aceita um próton, forma-se seu ácido conjugado. Na reação HCl + H₂O → H₃O⁺ + Cl⁻, o Cl⁻ é a base conjugada de HCl, e H₃O⁺ é o ácido conjugado de H₂O.
Já a teoria de Lewis vai além, definindo ácidos como receptores de pares de elétrons e bases como doadoras de pares de elétrons. Esta definição abrange reações sem transferência de H⁺, como quando NH₃ (doa par de elétrons) reage com BF₃ (aceita par de elétrons).
🔬 Amplie seu conhecimento: A teoria de Lewis é a mais abrangente e explica reações ácido-base que as outras teorias não conseguem explicar!

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
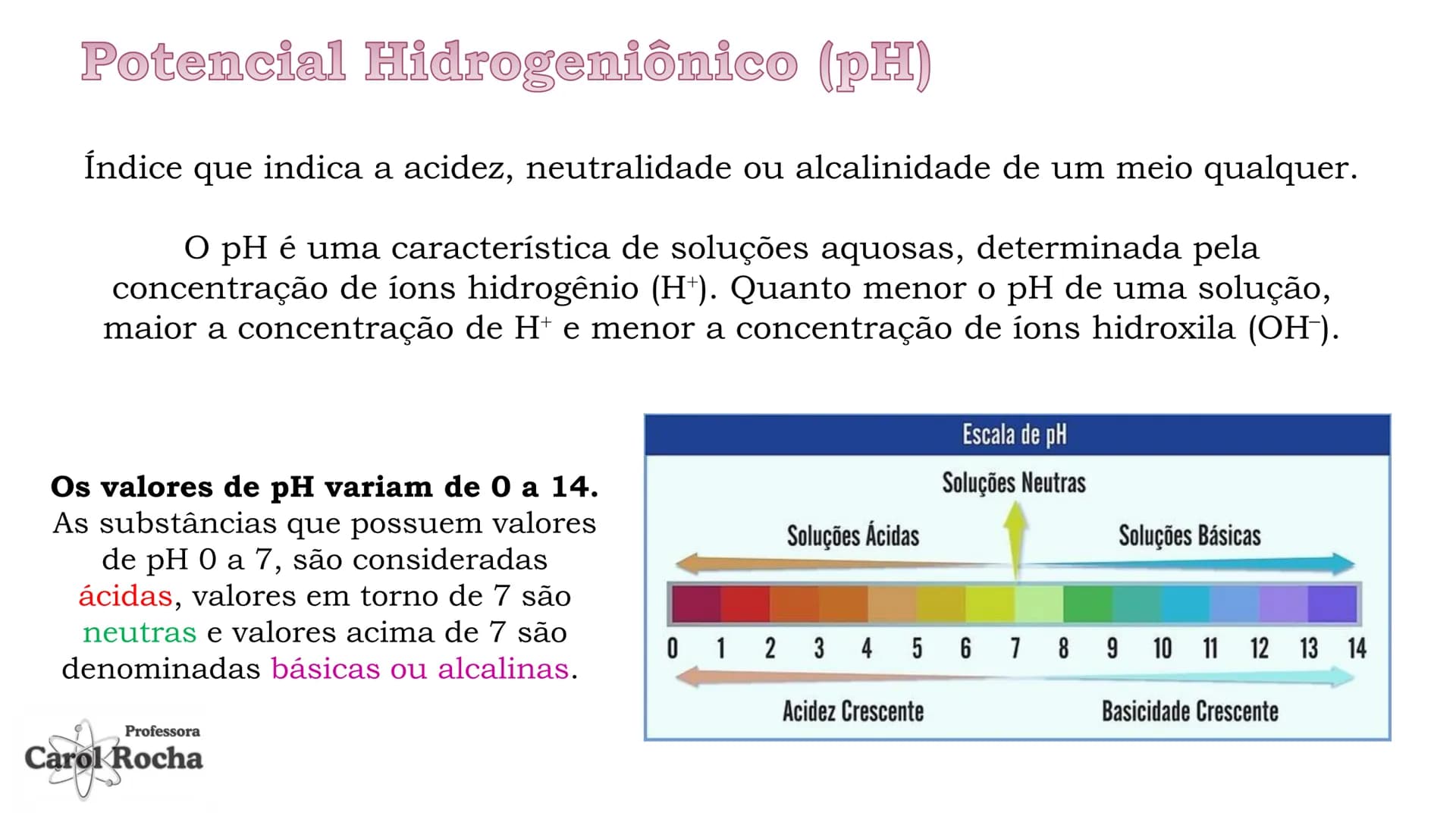
O potencial hidrogeniônico (pH) é uma escala que mede a acidez ou basicidade de uma solução. Variando de 0 a 14, o pH indica a concentração de íons H⁺ na solução: quanto menor o pH, mais ácida é a solução; quanto maior, mais básica.
Soluções com pH menor que 7 são ácidas (como limão, pH≈2), pH igual a 7 são neutras (água pura), e pH maior que 7 são básicas . Esta escala é logarítmica, então cada unidade representa uma mudança de 10 vezes na concentração de H⁺!
Para identificar o pH, usamos indicadores ácido-base, substâncias que mudam de cor conforme o pH do meio. A fenolftaleína fica incolor em meio ácido e rosa em meio básico, enquanto o papel tornassol azul fica vermelho em meio ácido e mantém a cor azul em meio básico.
🌈 Experimento caseiro: Use suco de repolho roxo como indicador natural! Ele fica vermelho em meios muito ácidos, roxo em meios neutros e verde/amarelo em meios básicos.

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes

Acesso a todos os documentos
Melhore suas notas
Junte-se a milhões de estudantes
Nosso companheiro de IA foi criado especificamente para atender às necessidades dos estudantes. Com base nos milhões de conteúdos que temos na plataforma, podemos oferecer respostas realmente relevantes e significativas. Mas não se trata apenas de respostas, o companheiro também está aqui para guiar você pelos desafios diários de aprendizado, com planos de estudo personalizados, quizzes ou conteúdos no chat e 100% de personalização com base nas suas habilidades e desenvolvimentos.
Pode descarregar a aplicação na Google Play Store e na Apple App Store.
Sim, tem acesso gratuito ao conteúdo da aplicação e ao nosso companheiro de IA. Para desbloquear determinadas funcionalidades da aplicação, pode adquirir o Knowunity Pro.
6
Ferramentas Inteligentes NOVO
Transforme esta anotação em: ✓ 50+ Questões de Prática ✓ Flashcards Interativos ✓ Simulado Completo ✓ Esquemas de Redação
App Store
Google Play
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS
O app é muito fácil de usar e bem projetado. Encontrei tudo o que estava procurando até agora e consegui aprender muito com as apresentações! Definitivamente vou usar o app para uma tarefa de classe! E, claro, também ajuda muito como inspiração.
Stefan S
usuário de iOS
Este app é realmente ótimo. Tem muitos materiais de estudo e ajuda [...]. Minha matéria problemática é o francês, por exemplo, e o app tem tantas opções de ajuda. Graças a este app, eu melhorei meu francês. Eu recomendaria para qualquer pessoa.
Samantha Klich
usuária de Android
Uau, estou realmente impressionado. Eu experimentei o app porque vi muitos anúncios e fiquei absolutamente maravilhado. Este app é A AJUDA que você quer para a escola e, acima de tudo, oferece muitas coisas, como treinos e resumos, que têm sido MUITO úteis para mim pessoalmente.
Anna
usuária de iOS
aplicativo PERFEITO! além de te ajudar a estudar de verdade (diferente do chatgpt que só te dá a resposta), tem vários quiz e outras atividades interativas pra ajudar a fixar ainda mais o conteúdo, tudo perfeito, meu novo app preferido!
S Dudah
usuário iOS
o aplicativo e incrível, eu sou estudante do primeiro ano, e estudei o ensino fundamental todo e uma escola que não tinha nem o básico pra educação, graças a esse aplicativo eu consegui chegar ao nível que estou, knowunity tem quiz de várias matérias e quando você erra uma eles explicam o por que de você está errada, os mapas mentais que tem são incríveis e o chat e bem explicativo.
Milena S
usuária Android
Esse app te ajuda a se preparar para as provas, e além do mais, ajuda outras pessoas, super recomendo esse app, podem baixar sem medo algum! 💖
David K
usuário iOS
O app é simplesmente incrível! Só preciso digitar o assunto na barra de pesquisa e recebo a resposta bem rápido. Não preciso assistir a 10 vídeos no YouTube para entender algo, assim economizo meu tempo. SUPER RECOMENDO!
Sudenaz Ocak
usuário Android
Na escola eu era muito ruim em matemática, mas graças ao app, estou indo melhor agora. Sou muito grato por você ter criado o app.
Bonnie dando o sinal verde
usuária de Android
Eu particularmente amei pra aquele aluno que odeia ver no livro justifique sua resposta ,e só vc pergunta pra ele uma resposta pessoal dele que ele responde meu novo melhor amigo ele me deixou muito segura para as provas
Julia S
usuária Android
Vi esse aplicativo no TikTok, e resolvi baixar pois estava na semana de testes E ME AJUDOU MUITO, Além de me ajudar nos deveres escolares me ajudou nos teste e está me ajudando nas provas bimestrais 🩷
Marco B
usuário iOS
OS QUIZ E CARTÕES DE ESTUDO SÃO MUITO ÚTEIS E EU AMO A IA DO Knowunity. TAMBÉM É LITERALMENTE COMO O CHATGPT MAS MAIS INTELIGENTE!! ME AJUDOU COM MEUS PROBLEMAS DE RÍMEL TAMBÉM!! E COM MINHAS MATÉRIAS DE VERDADE! ÓBVIO 😍😁😲🤑💗✨🎀😮
Sarah L
usuária Android
Ajuda em todas as matéria e ainda replica como resolver, eu amei, aprendi muita coisa de matemática, e o melhor app de estudos
Lucia
usuário iOS